Cancer Cell | 發現PAI-1阻斷放射免疫治療遠端效應的分子機制_風聞
葆力医学观察-专注生物科研领域,趣味科普与行业干货齐飞1小时前
放射免疫治療的遠端效應,即腫瘤縮小發生在照射野之外,在治療上很有希望,但臨牀上很少見。這種效應背後的機制仍不清楚。
2025年3月13日,南方醫科大學董忠誼、Wu De-Hua、Bai Xue、Guan Jian共同通訊在Cancer Cell(IF=48.8)在線發表題為“PAI-1-driven SFRP2high cancer-associated fibroblasts hijack the abscopal effect of radioimmunotherapy”的研究論文,該研究發現PAI-1驅動的SFRP2high腫瘤相關成纖維細胞阻斷放射免疫治療的遠端效應。 該研究使用體內全基因組CRISPR篩選確定SFRP2是潛在的基質調節因子。SFRP2在未接受放射治療的腫瘤中表現出癌相關成纖維細胞(CAF)特異性表達和放射免疫療法介導的上調。
CAFs中條件性Sfrp2敲除通過重新構建血管免疫微環境來促進CD8+T細胞募集到未照射的腫瘤中,從而增強了遠端效應。體內譜系追蹤顯示SFRP2升高與放射免疫治療驅動的周細胞譜系承諾相關。血清蛋白質組學顯示,放射腫瘤分泌的PAI-1通過LRP1/p65軸觸發遠處腫瘤周細胞命運轉變為SFRP2high CAFs。藥理學阻斷SFRP2或PAI-1增強人源化患者異種移植模型中的膿腫效應。該發現説明了PAI-1誘導的SFRP2high CAFs作為關鍵的基質調節因子來抑制遠端效應,為增強放射免疫治療的效果提供了有希望的靶點。

放射治療(RT)在多種癌症疾病的臨牀管理中仍然至關重要,經常用於靶向局部或寡轉移病灶。RT還可以通過刺激遠端效應表現出更廣泛的全身性和有效的抗癌能力:腫瘤特異性免疫反應影響遠處的未照射轉移,導致其消退。此外,這種特性可以通過使以前無反應的腫瘤對這種傳統的基於藥物的治療敏感來增強免疫檢查點抑制劑(ICI)的有效性。儘管將放射治療與免疫治療(即放射免疫治療)相結合的前景看好,但遠端效應很少發生在現實世界中。
自Robin Moles於1953年提出其最初建議以來,已經進行了許多努力,如增加腫瘤免疫原性,增強腫瘤引流淋巴結(TDLNs)中的T細胞啓動,對遠端腫瘤應用低劑量輻射,和系統地激活抗腫瘤巨噬細胞,以增強遠端效應。然而,目前的研究主要是假設檢驗,具體的目標仍然探索不足。此外,將臨牀前發現轉化為臨牀觀察不一致,可能是因為現有的腫瘤模型不能準確地複製人類生物學。
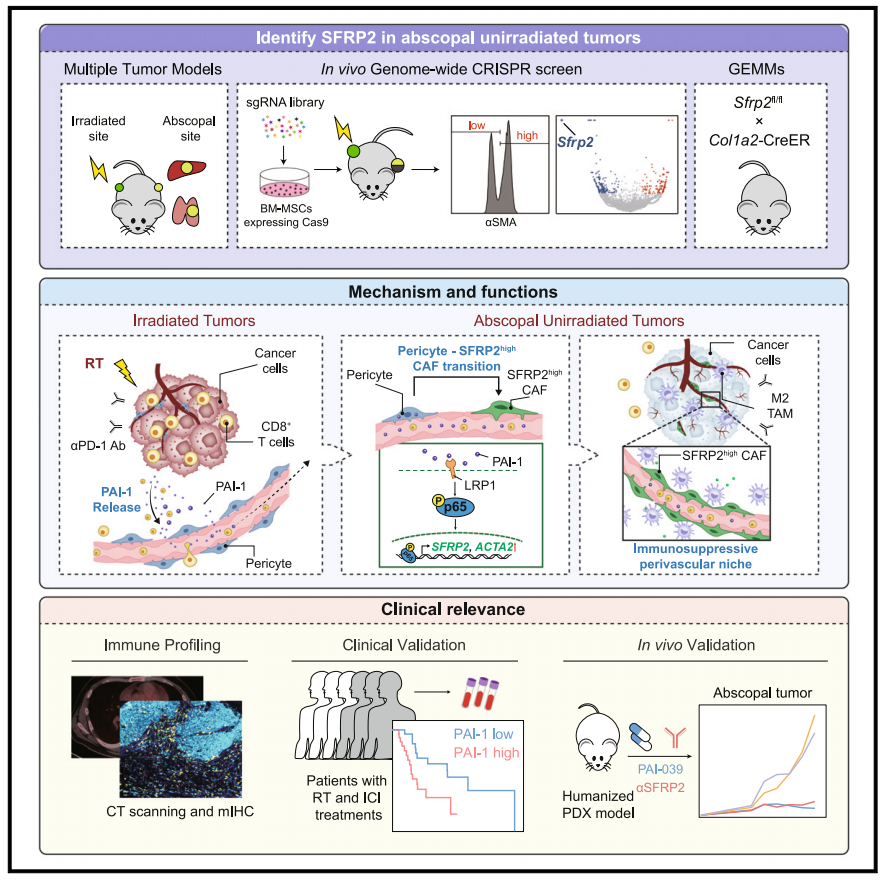
機理模式圖(圖源自Cancer Cell)
在這裏,研究人員使用CRISPR全基因組編輯實現了一個正向遺傳篩查,以研究遠端特異性遺傳弱點。研究發現SFRP2high腫瘤相關成纖維細胞(CAFs)通過塑造血管周圍的免疫抑制小生境,從而阻止CD8+ T細胞募集到未受照射的腫瘤中,從而控制了遠端效應。此外,輻射腫瘤釋放的PAI-1通過血流到達遠端腫瘤,在那裏誘導周細胞-成纖維細胞轉化(PFT)產生SFRP2high CAFs。阻斷SFRP2信號傳導級聯可以在人源化患者異種移植(PDX)模型中觸發放射免疫治療的遠端效應。
原文鏈接:https://www.cell.com/cancer-cell/fulltext/S1535-6108(25)00076-5