抗衰“避坑指南”:科學家發佈最新延壽路線圖,揭秘抗衰真相與五大困境_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯58分钟前

“100歲(這個目標)太低了,讓我們再把這個數字翻幾倍!”
2024年,在美國米爾肯研究所舉辦的全球大會上,XPRIZE基金會創始人、63歲的億萬富豪Peter Diamandis的豪言引發全場沸騰,台下掌聲雷動,彷彿人類戰勝衰老的未來已經觸手可及。

市場數據也印證着這份狂熱。2023年,全球抗衰老和長壽市場規模達到大約636億美元,2024-2030年間還將以21.5%的年均複合增長率持續擴大。從硅谷到華爾街,從生物科技初創企業到傳統制藥巨頭,無不在押注這個新賽道。
但在這片繁榮景象的背後,一個殘酷的現實往往被忽視:目前絕大多數的"長壽干預方案",要麼停留在實驗室階段,要麼沒有經過長期、可重複驗證的臨牀檢查,真正有效的方案依然寥寥無幾。
在資本狂熱與科學驗證嚴重脱節的背景下,呂宇軒、餘丹陽、曾心怡、David Barzilai與Dominik Thor幾位衰老研究學者,昨日聯合發佈了一份題為《Bridging expectations and science: a roadmap for the future of longevity interventions》長壽路線圖,系統構建了長壽干預手段從實驗室走向臨牀的關鍵轉化路徑[1]。
這不僅是科學對泡沫的回應,也是一份為行業釐清邊界、重建信任的行動指南。


當我們談論抗衰老時,我們究竟在談論什麼?
在科學語境中,壽命、健康壽命、長壽、抗衰這些術語,各自有着清晰而明確的定義。
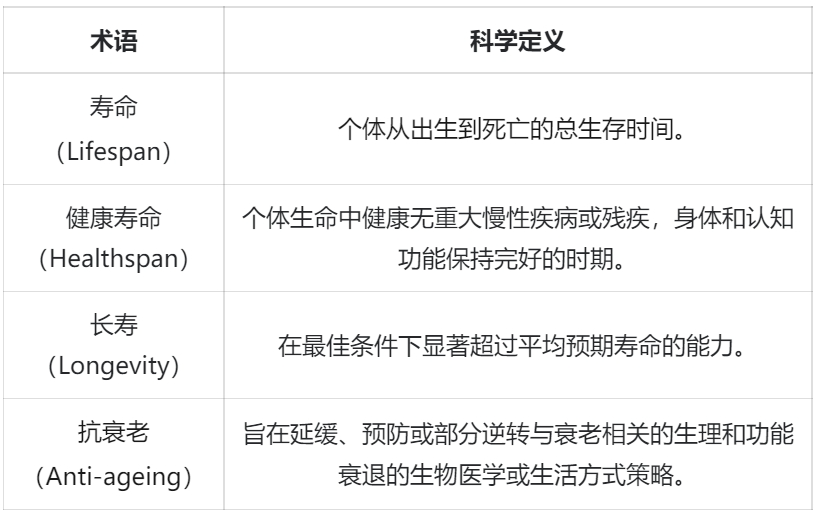
然而,科學有科學的定義,大眾有大眾的理解。
在現實生活中,這些術語常被混用,並在不同人眼中意味着完全不同的東西:有人追求長壽,有人渴望“凍齡”,也有人只是希望遠離病痛、保持活力。
那麼,當我們談論抗衰時,我們究竟是在談論什麼?
No.1
健康
調研顯示,若身心健康能得到保障,79.7%的受訪者希望壽命超過120歲,超過半數的人願意無限延長壽命。然而在無法保證健康的情況下,65.3%的人寧願只活到85歲。
這表明延長壽命的前提是延長健康壽命,比起活得久,人們更關注能否活得好。
No.2
實際的益處
對營養補劑行業的實證研究顯示,消費者更看重改善身體功能、降低疾病風險、外觀年輕化等切實的健康益處,而非抽象的衰老生物標誌物變化。
雖然衰老生物標誌物如表觀遺傳時鐘和端粒長度等常用來衡量生理年齡和疾病風險,但由於個體和組織差異較大,短期干預效果不明顯,現階段缺乏臨牀驗證用於指導干預。
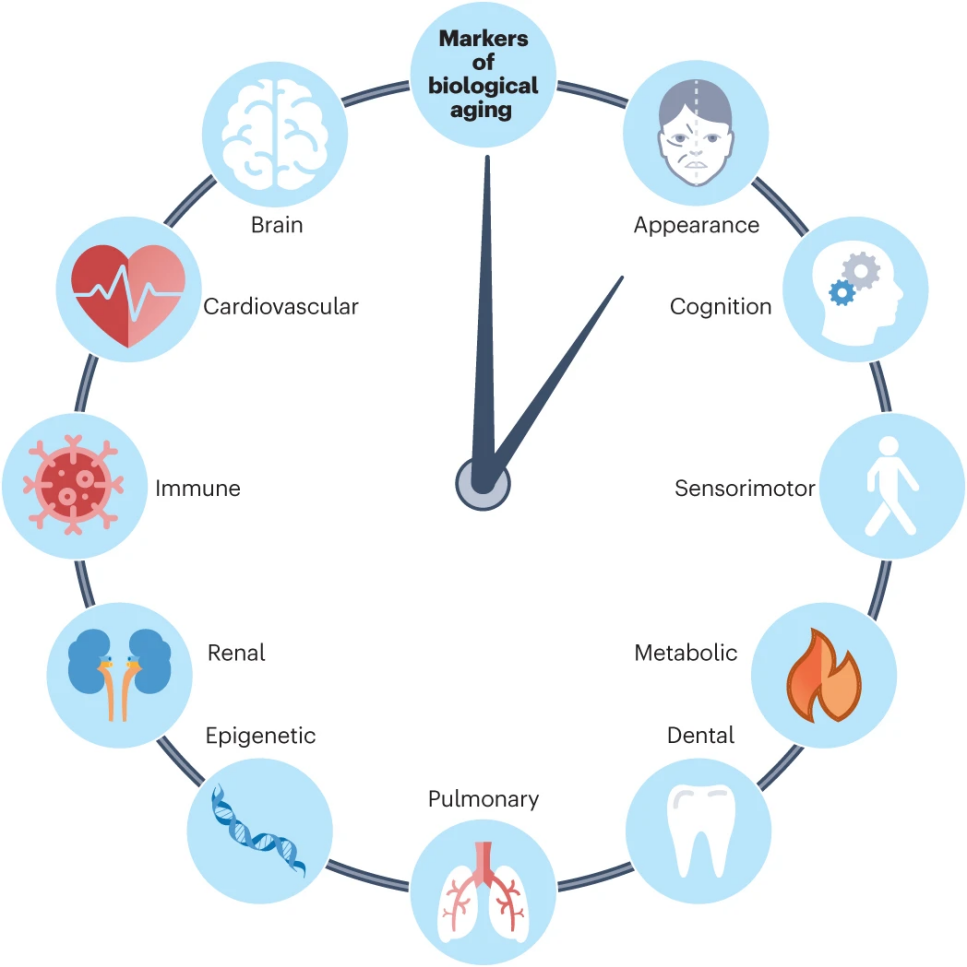
圖注:多個器官系統中的生物標誌物可用於預測一個人的生理年齡[2]
No.3
多元的目標
人們的抗衰目標,會隨着年齡、性別等因素的不同出現差異。
年輕人(18-29歲)希望將外表“凍齡”在23歲左右,老年人(60歲以上)則更注重延長健康壽命減輕衰老相關疾病負擔。男性通常更願意嘗試壽命延長的技術,而女性則更主導了抗衰老美容產品市場。
No.4
安全至上
大眾對長壽干預手段的接受程度,主要取決於他們對其安全性和副作用風險的認知。
因此,相比藥物(如二甲雙胍26%、雷帕黴素10%),人們對運動(66%)與補劑(82%)的接受度顯著更高,而對幹細胞療法、血漿置換等激進且實驗性干預手段則普遍持謹慎態度。
儘管補劑被認為風險較低,但許多市售產品缺乏長期臨牀安全和有效性驗證,甚至可能有害,例如2024年日本發生的“紅曲米事件”——小林製藥生產的紅曲米補劑,引發約3000起不良反應,甚至包括多例急性腎衰竭致死。

從實驗室到臨牀干預的五大障礙
儘管公眾熱情高漲,資本湧入,衰老研究不斷發展,但要將這些前沿干預方法落地並廣泛應用,依然面臨多重挑戰。
No.1
心理障礙:信任危機與認知偏差
儘管抗衰老研究取得了顯著進展,公眾對相關干預措施的信任度仍然偏低。
一方面,在歷史上許多未經充分驗證的“抗衰老療法”誇大了其效果,使得消費者對新興技術產生了懷疑;
另一方面,科學研究的轉化難題同樣不容忽視。**許多在動物實驗中取得的成功,往往難以直接應用到人類身上。**人們感知到的益處,往往源於安慰劑效應或健康行為的改善,而非真正的治療效果。
No.2
經濟障礙:高昂成本與可及性困境
高昂的成本是長壽醫學普及的主要障礙。
以基因療法為例,FDA批准的首個CRISPR療法Casgevy定價高達220萬美元,競爭對手Lyfgenia的價格則為310萬美元。儘管這些療法展現出巨大潛力,但由於其高昂的價格,並且目前僅針對特定疾病治療,難以廣泛應用於預防或逆轉衰老。
而成本較低的雷帕黴素和二甲雙胍等藥物,雖然在臨牀前模型中展示出抗衰老潛力,但因未獲得相關監管批准,且大多數健康保險不予覆蓋,仍需自費購買。
No.3
實踐障礙:技術與轉化瓶頸
目前,各類干預措施,包括營養補劑、藥物、基因療法、幹細胞治療及其衍生物等,雖然在部分研究中展示了抗衰潛力,但仍缺乏系統的臨牀試驗數據支持。
在實際轉化過程中,規模化生產、標準化工藝和質量控制等問題尤為突出,特別是幹細胞和外泌體等複雜生物製劑的穩定性和一致性控制,這些瓶頸限制了干預手段從實驗室向臨牀的轉化。

圖注:從實驗室研究到臨牀應用之間,存在一個被稱為“死亡之谷”的過渡階段,充滿各種挑戰[3]
No.4
溝通障礙:科學傳播與消費者期望的錯位
雖然消費者偏好具體、可見的健康益處,但他們同樣期望簡單、直接的指標來解釋健康結果。
然而,類似的生物標誌物的開發面臨多重挑戰,包括缺乏標準化的生理年齡定義、數據源的可重複性問題,以及如何確保這些標誌物在臨牀中的實際效用。
與此同時,複雜的科學發現常在傳播中被過度簡化或炒作,導致不切實際的期望,並掩蓋了科學的不確定性。一些商業化的長壽干預方法,雖然缺乏嚴謹的證據支持,卻通過誤導性營銷推向市場,進一步加劇了公眾的誤解。
No.5
監管障礙:監管空白與標準缺位
長壽領域目前處於監管模糊地帶,許多幹預措施(如生理年齡檢測、衰老細胞清除藥物、長壽診所等)在不完善的監管框架下運作。
全球監管差異也加劇了臨牀採納的複雜性,如歐洲藥品管理局對臨牀試驗和長期驗證有着嚴格的要求,導致審批較慢;而澳大利亞等監管寬鬆的國家,雖能夠加速創新,但也存在過早商業化的隱患。
監管不明和執法不力使得未經驗證的“抗衰老”產品氾濫,進而加劇虛假宣傳和消費者信任危機。
此外,雖然衰老生物標誌物與多種疾病密切相關,但是否將衰老視為可改變的狀況仍無共識,這限制了藥物的開發。
為確保安全並建立信任,衰老生物標誌物驗證應採用標準化框架,並推行FAIR數據原則(可發現、可訪問、可互操作、可重用),以提高透明度,減少誤導信息和選擇性報告。

科學破局路線圖
為打破障礙,科學家們描繪出一份清晰的路線圖,旨在解決長壽干預措施從實驗室到臨牀的轉化難題,指引前行的方向。
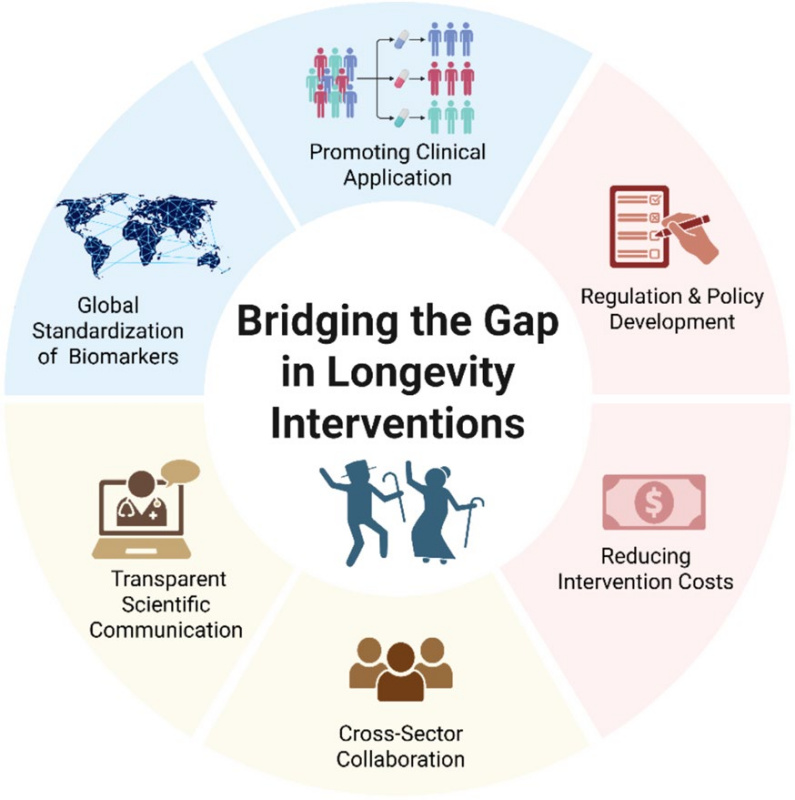
圖注:路線圖
No.1
整體干預與還原論干預
為了打破消費者的心理障礙,長壽干預應優先採用多維度的綜合策略,強調改善整體生活方式(如規律運動、合理飲食和積極社交等),而非僅依賴單一的分子療法,優先考慮那些通過隨機對照試驗驗證的方式,而非僅依賴分子或臨牀前的指標,這樣做有助於減少歷史上過度承諾帶來的懷疑。
同時,應公開透明地傳達基於證據的干預效果,避免誇大其詞,且坦誠地討論侷限性和倫理問題,建立公眾信任。
No.2
生物標誌物在臨牀中的應用
為了滿足消費者對健康益處的需求,衰老生物標誌物的研究應通過嚴格的臨牀驗證與實際可操作的干預措施相結合。
這一過程需要建立在前瞻性臨牀研究基礎之上,確保生物標誌物與健康結果之間的明確關聯,而非僅停留在相關性或替代終點數據上。
儘管複合生物標誌物在羣體層面的預測潛力顯現,但其在個性化干預中的有效性仍需進一步驗證。
為提高生物標誌物的可及性,開發經濟高效的治療和診斷工具,並推動其在保險中的覆蓋至關重要。此外,科研人員、臨牀醫生、政策制定者及其他相關方之間的合作,能夠確保科學創新與實際需求相匹配。
No.3
衰老生物標誌物的全球標準化
衰老生物標誌物的全球標準化對臨牀轉化至關重要。
由於方法學差異和人羣普遍性的侷限性,目前尚無生物標誌物得到FDA等監管機構的正式認證作為替代終點。為此,中國衰老標誌物研究聯合體(Aging Biomarker Consortium)和衰老生物標誌物國際聯盟(Biomarkers of Aging Consortium)等正在努力建立共享的驗證標準。
在這個過程中,現有國際框架為我們提供了有益的參考:世界衞生組織(WHO)通過專家小組推動全球共識,人用藥品技術要求國際協調理事會(ICH)則提供了統一的監管指導原則(如E6良好臨牀規範與E9臨牀試驗統計原則)。
為了實現這個目標,監管機構(如FDA、EMA、PMDA)、全球衞生組織(如WHO、ICH)、研究聯盟和行業等應通力合作,通過專家共識、共享數據庫和公私合作來促進這一進程。建議分階段推進:
短期:共識建設和數據協調;
中期:研究驗證和監管參與;
長期:整合至臨牀試驗並實現正式認證。
No.4
科學傳播
研究人員應與患者倡導者合作,開發面向公眾的教育項目,通過社交媒體平台傳播科學可信的信息,將衰老研究轉化為可應用的干預措施。
一項歐洲調查顯示,只有16%-20%的受訪者認為大眾媒體是傳播科學社會影響的首選渠道,63%的受訪者更傾向於通過研究人員獲取信息。
因此,研究人員應積極與公共傳播者合作,利用社交媒體等平台準確且深入地解釋長壽科學,幫助公眾更好地理解長壽干預中的科學不確定性。
有研究表明,社交媒體的快速消費模式可能讓用户對複雜的健康信息失去興趣。為了應對這個問題,研究人員還需要根據這些特點調整傳播策略,確保公眾能夠持續關注並真正理解內容。
No.5
監管指南
清晰一致的監管指南對於將長壽干預安全地引入臨牀實踐至關重要。
目前,全球尚未統一對於衰老的定義,也缺乏經過驗證的替代終點,如果能就衰老相關的臨牀結果(如衰弱、功能衰退或分子標誌物)達成共識,將為試驗設計和監管評估提供堅實的基礎。
為了推動這一進展,現有的國際框架,如ICH和WHO,可以作為良好的起點。例如,TAME試驗通過功能終點來評估二甲雙胍對年齡相關疾病的影響,在此基礎上,可以成立類似ICH工作組的國際專門團隊,幫助統一衰老生物標誌物、結果測量和倫理監督的標準。
這一進程需要監管機構(如FDA、EMA、PMDA)、研究聯盟(如BAC、Geroscience Network)、全球衞生組織(如WHO、OECD)以及行業各方的緊密合作,共同制定長壽干預的監管指南,並通過將衰老研究納入國家系統和全球註冊平台(如WHO ICTRP),提高試驗的透明度。
建立這樣的流程,不僅有助於確保新幹預措施達到高標準的安全性和有效性,還能加速長壽科學領域的創新。
抗衰老領域正處於一個十字路口。一邊是無限膨脹的市場預期,將“長生不老”包裝成觸手可及的商品;另一邊是科學家們冷靜勾勒的路線圖,提醒我們謹慎跨越實驗與臨牀之間的“死亡之谷”。
這樣一份科學的長壽干預路線圖的出現,有助於讓抗衰從資本敍事迴歸科研本質。
真正的抗衰老革命,往往不是來自某一項神奇的突破,而是構建一個科學證據、倫理責任與個體需求共振的生態系統。只有這樣,長壽的願景才能從實驗室走向現實,使一個更健康、可持續的未來成為現實。
聲明 - 本文內容僅用於科普知識分享與抗衰資訊傳遞,不構成對任何產品、技術或觀點的推薦、背書或功效證明。文內提及效果僅指成分特性,非疾病治療功能。涉及健康、醫療、科技應用等相關內容僅供參考,醫療相關請尋求專業醫療機構並遵醫囑,本文不做任何醫療建議。如欲轉載本文,請與本公眾號聯繫授權與轉載規範。
參考文獻
[1] Yu, D., Zeng, X., Barzilai, D., Thor, D., & Lyu, Y.-X. (2025). Bridging expectations and science: a roadmap for the future of longevity interventions. Biogerontology, 26(4), 1–12. https://doi.org/10.1007/s10522-025-10278-z
[2 ]May, M. (2023). Biomarkers of aging remain elusive as researchers try to slow the biological clock. Nature Medicine, 29(11), 2673–2676. https://doi.org/10.1038/s41591-023-02560-9
[3] Butler, D. (2008). Translational research: Crossing the valley of death. Nature, 453(7197), 840–842. https://doi.org/10.1038/453840a