最高延壽17.6%!比甲基化時鐘更早一步,僅需30天,搞定篩藥全流程!_風聞
时光派-时光派官方账号-聚集全球前沿、全面、专业抗衰资讯49分钟前

既要花費數年光陰,又要燒掉百萬經費,結果還不一定如人所願?這種事情乍一聽就沒人愛做,但這卻是藥物研發的“常規操作”。抗衰藥也同樣:從上千種候選藥物裏,找出延壽的那一個,然而每一個選擇都無異於一場豪賭……
雖面臨如此困境,但來自哈佛醫學院的Gladyshev團隊,為破解這一難題提供了個全新的方案[1]:利用其獨創的“長壽分子指紋”平台,僅需一個月的細胞實驗與短期動物測試,就能精準預測出真正具有延壽潛力的化合物。
派派在這也劇透一波:就在今年9月即將開幕的時光派第六屆衰老幹預論壇上,派派有幸邀請到了本文兩位作者——美國國家科學院院士Vadim Gladyshev教授與甲基化時鐘之父Steve Horvath教授。屆時,我們將有機會聆聽他們有關長壽分子的最新見解!點擊下方卡片,後台回覆關鍵詞 第六屆 獲取論壇報名通道~

長壽分子指紋的“前世今生”
物理學家們做夢都想用一個公式拿捏整個宇宙——大統一理論。
那麼,在衰老過程複雜多變的分子機制中,是否存在“大統一理論”呢?這個設想並非憑空而來,哈佛醫學院的Vadim Gladyshev教授及其團隊,正是這一問題的堅定求索者。
此靈感最早來源於他們團隊在 2017 年的一項成果[2]:無論是天生就巨能活的“老天爺賞飯吃”型物種(如裸鼴鼠、弓頭鯨),還是在實驗室裏通過“後天努力”(如熱量限制等干預手段)續命成功的動物,它們體內都呈現出相似的分子特徵!
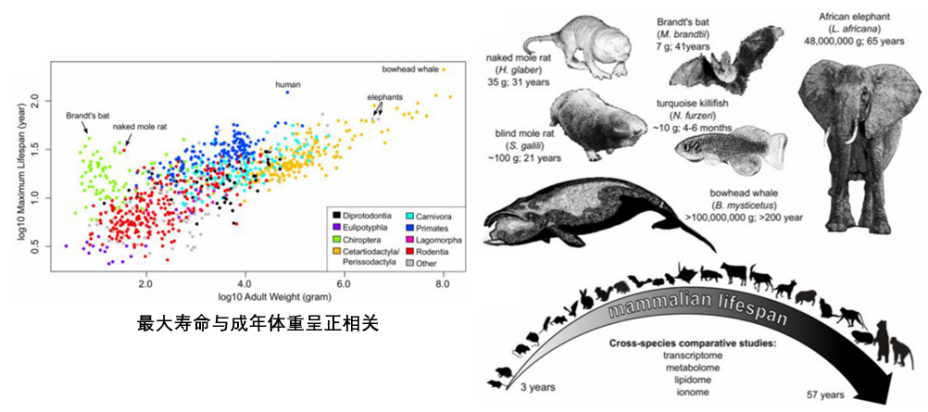
比如説,它們都擁有更牛掰的 DNA 損傷修復能力與一套獨特的免疫應答模式(儲備了更多樣、更強大的免疫基因)。
這些強大的能力並非憑空而來,而是體現在了基因的活動層面。在耗時近十年的求索過程中,科學家們發現:任何延壽方法,似乎都是在塑造一套獨特的基因表達模式(關於氧化應激、線粒體代謝和DNA修復、免疫和炎症等相關基因的表達),它們就類似於基因的“指紋”。
為了驗證並完善這一理論,Gladyshev團隊進行了一系列研究、分析了多種小鼠延壽干預措施帶來的基因表達變化過程。最終,他們成功繪製出首個相對清晰的“長壽指紋”圖譜,並證明了它具備預測新藥的潛力[3]。
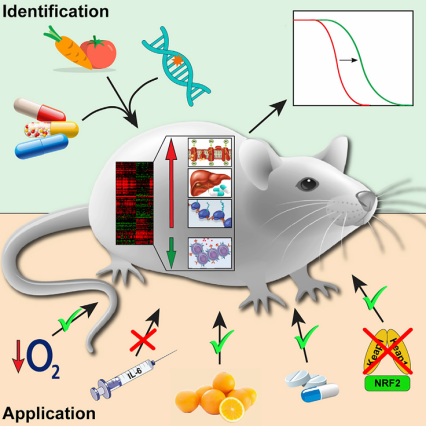
圖注:通過分析多種已知延壽方法(如飲食、藥物)的共同分子特徵,科學家們成功繪製出了一套長壽分子指紋(紅綠相間的熱圖),用來快速篩選和評估新的潛在抗衰老幹預措施
隨後,他們又將研究版圖擴張至上百種哺乳動物,這也帶來了一個核心發現[4]:在所有組織中,與“翻譯保真度”相關的通路(細胞內確保蛋白質被正確合成的質量管控體系),其基因表達水平越高,物種的壽命則越長。
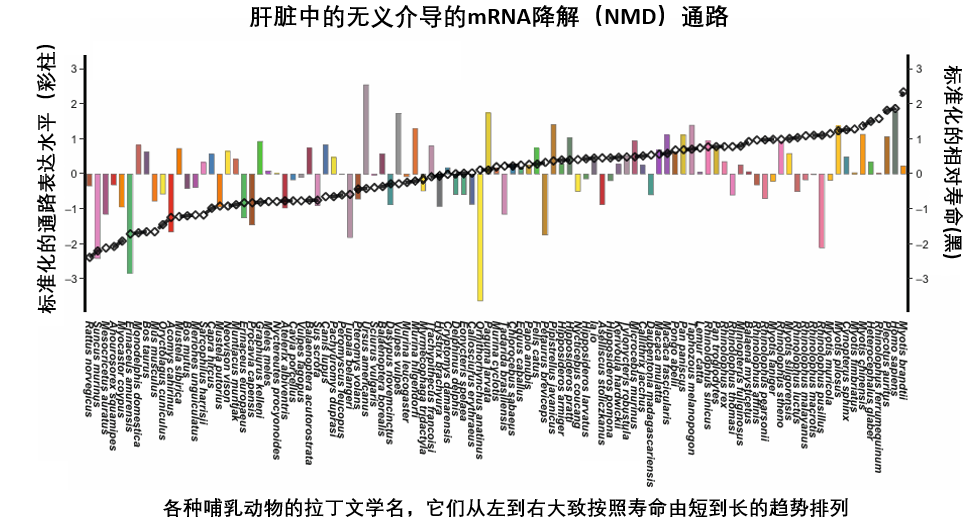
圖注:一個高效、強大的NMD通路,能最大程度地減少錯誤蛋白質的產生,維持細胞內部環境穩態
因此,維持蛋白質合成的精確性,很可能是哺乳動物在進化中保留下來的、實現長壽的核心保守策略之一,科學家們也因此能更自信地將其整合進篩選平台中,並將“上調翻譯保真度通路”作為篩選藥物時的一個核心權重指標。

至此,歷經近十年的積累和迭代,Gladyshev團隊手中已握有一套經過反覆驗證、不斷完善的“長壽分子指紋”識別系統。那麼,作為一個抗衰藥物篩選引擎,它究竟是怎樣具體實施的?

四步篩選法
為了更好篩選藥物,Gladyshev團隊設計了一個四步篩選法:
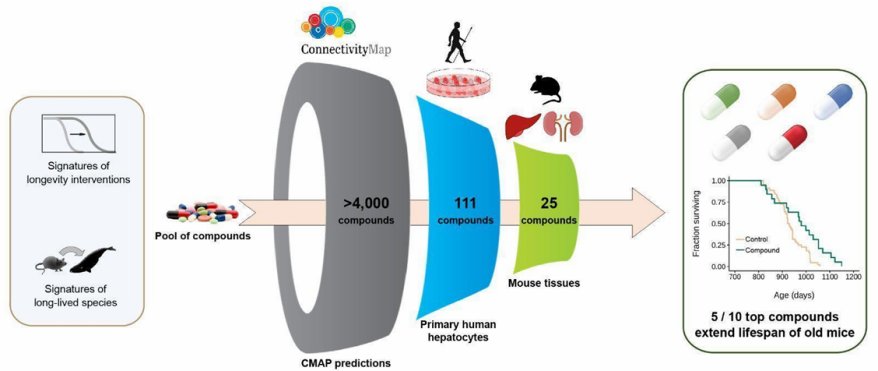
第一步——計算機模擬篩選:利用數據庫,科學家們從超過4000種化合物中初篩出111名“種子選手”,這些都是被認為能誘導出“長壽指紋”的潛力股!
第二步——細胞驗證:科學家們將這111種候選物分別用在人類原代肝細胞(PHH)上,不僅考查它們的安全性,還要在細胞水平上選拔出基因變化符合“長壽指紋”的物質。範圍進一步縮小,有25種藥物脱穎而出。
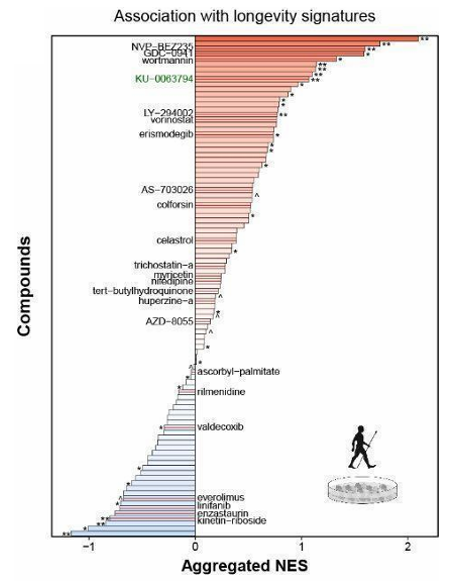
圖注:這些化合物依據它們與長壽模式的關聯分數(Aggregated NES)從高到低被排好序
第三步——動物驗證:Gladyshev團隊在年輕雄性小鼠身上測試了這25個物質,持續1個月。結果顯示,10款得分最高的物質(它們在肝、腎中均誘導了高度一致的分子效應,表明其普適性)成功復刻了最接近“長壽指紋”的分子變化,進入最終階段。
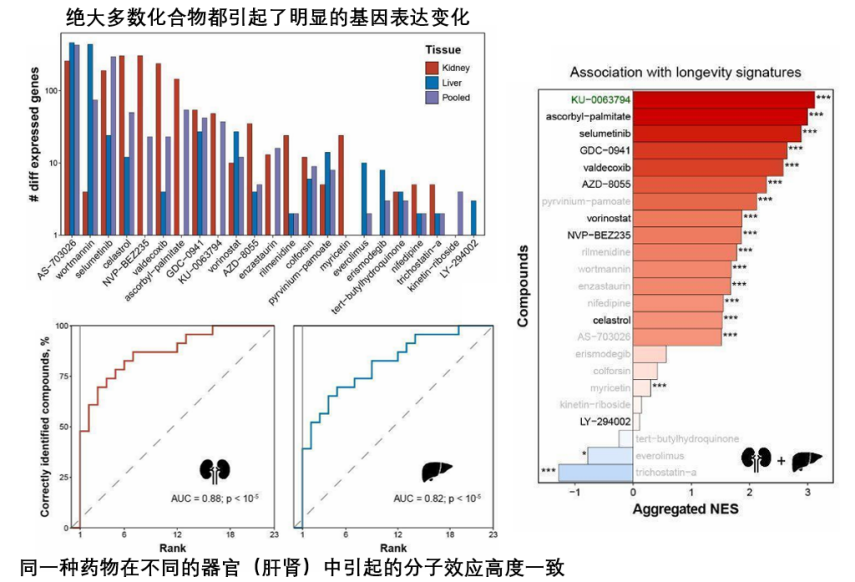
第四步——延壽實戰:這也是真正的壽命實驗。科學家們將這10種藥物,分別餵食給老年小鼠(相當於人類的70-80歲),記錄下它們的壽命。最終,共有5種藥物顯著延長了老年雄性小鼠的壽命和健康期。
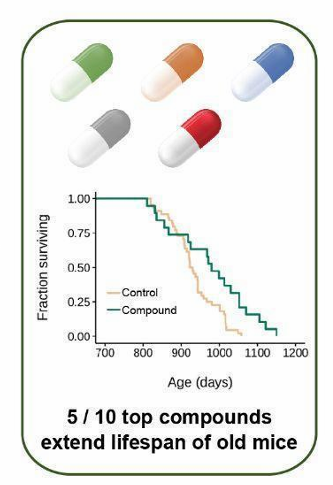

10選5,延壽效果看得見!
那麼,這5種從111種化合物中脱穎而出的抗衰藥預備役究竟是何方神聖,有沒有驚喜呢?讓我們一個個來看:
No.1
經典長壽通路的再次勝利:LY-294002(PI3K抑制劑)& AZD-8055(mTOR抑制劑)
這倆可以放在一起看,它們是藥物研發領域研究成熟的工具藥,雖然它們作用靶點略有不同,但都成功抑制了最經典的PI3K/mTOR通路(雷帕黴素就是通過抑制mTOR來延壽的),分別使半數小鼠的壽命延長了8.7%與10.9%。
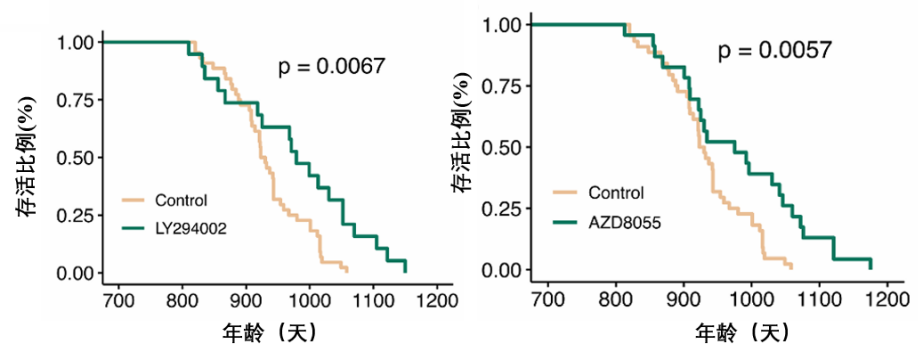
No.2
天然化合物:Celastrol(雷公藤紅素)
除了人工合成的抗衰候選藥物,還有大自然的饋贈。Celastrol(雷公藤紅素)是一種具有強大抗炎作用的天然化合物,在本次實驗中,它成功將半數小鼠的壽命延長了約6.5%。
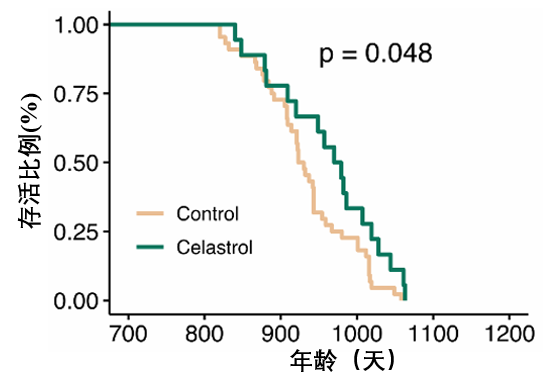
No.3
老藥新用:Selumetinib(MEK1/2抑制劑)、Vorinostat(HDAC抑制劑)
作為已經上市的抗癌藥物,它們的抗衰秘訣與其抗癌本行一脈相承:Selumetinib能阻斷關鍵的細胞生長通路,不僅抑制腫瘤,還能帶來8.7%的壽命增長;而作為表觀遺傳調節劑的Vorinostat則專注於提升健康壽命,改善小鼠的健康狀況。
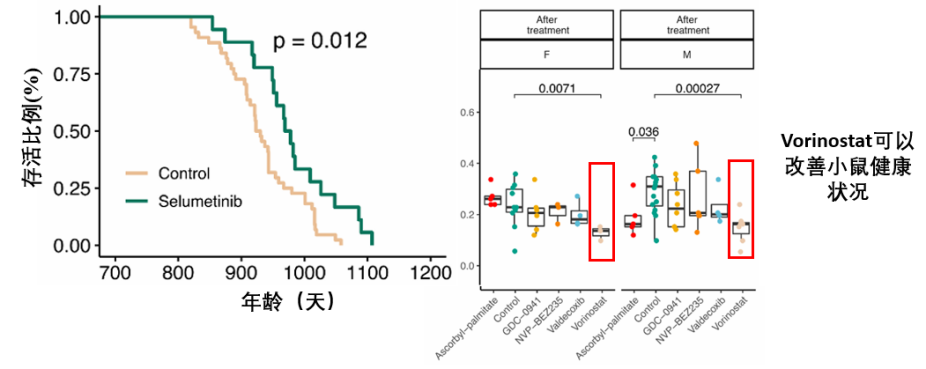
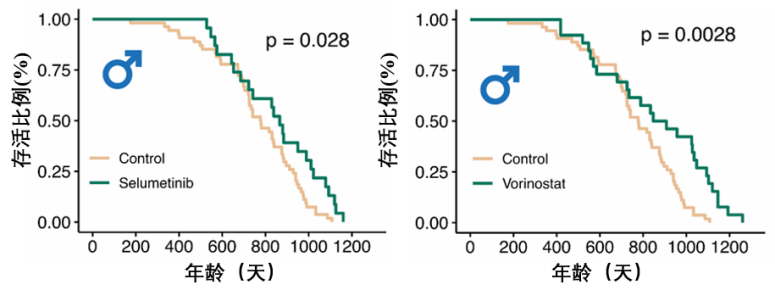
為了證明這些發現並非偶然,科學家們開始了二次驗證,結果再次傳來捷報:延壽成功的Selumetinib、僅改善健康的Vorinostat,依然成功地延長了雄性小鼠的壽命(前者延壽11.8%,後者則為17.6%)。
最後,科學家們又使用了DNA甲基化時鐘測試生理年齡,發現Selumetinib成功逆轉了小鼠心臟的表觀遺傳年齡。也就是説,能誘導“長壽指紋”的藥物的的確確能帶來基因上的年輕!
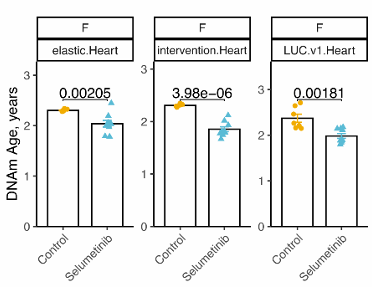
圖注:Selumetinib不僅能延長壽命,還能在分子層面逆轉特定器官的表觀遺傳衰老
但這裏還有一點得説清楚,“長壽指紋”可不是DNA甲基化時鐘的翻版,甲基化時鐘值反映了衰老的基因最終狀態,而“長壽指紋”卻是揭示細胞在衰老過程中正在做什麼(是分子層面會發生什麼的動態變化),對於找到真正的抗衰藥物來説,再“透明”不過了。

圖注:甲基化的結果表明:到目前為止,你身體裏所有與衰老相關的分子變化(損傷、修復等)累積在一起,最終呈現出的結果就是:生物學年齡26歲
而DNA甲基化時鐘可以作為“長壽指紋”的強大互補工具:長壽指紋在早期篩選中預測藥物的機制潛力(分子變化是否更加年輕),甲基化時鐘則用於確認藥物的逆齡效果。
正如開頭所説,在過去,尋找抗衰老藥物的過程更像是一種充滿不確定性的“煉丹術”。科學家們往往依賴零散的線索、個人經驗,甚至是運氣,在一個又一個潛在藥物上進行漫長而昂貴的試錯。這種模式不僅效率低下,且成功率極難保證。

而Gladyshev團隊依靠“長壽指紋”這個金標準,直接把藥物發現這事,從依賴經驗和運氣的單點嘗試,轉變為了一個有章可循,還能不斷豐富的系統工程。過去需要數年才能得到的結果,如今僅需短短幾個月就可以做到!
這種能加速、能省錢、還能大規模流水線使用的buff疊滿的平台化能力,也讓ChatGPT之父、OpenAI創始人Sam Altman,看上了它背後的商業價值。

Sam Altman一向看不慣大多數公司的“龜速”,他認為,這個領域需要的是“ChatGPT式的速度與努力”。為了將這一理念付諸實踐,他個人豪擲1.8億美元,投資了抗衰老初創公司Retro Biosciences,並立了個Flag:“把人類健康壽命延長10年”。

而不得不提的是,本研究的共同第一作者Shindyapina博士和Tyshkovskiy博士,在研究工作完成後選擇雙雙離開哈佛,加盟Retro並持有了該公司的股份。如果説Altman的投資完成了戰略佈局,那麼Gladyshev團隊核心成員的加入,則是注入了實現這一戰略的核心能力。

當然,這無疑是一次精準的雙向奔赴,當最聰明的頭腦與最大膽的資本相遇,其產生的化學反應令人期待。而本篇研究,或許正是那塊即將推倒整個行業傳統研發模式的第一塊多米諾骨牌。
在2025年9月20~21日、時光派第六屆衰老幹預論壇即將隆重開幕之際,Gladyshev與Horvath教授就會為大家帶來一場精彩絕倫的演講。參加本次論壇,你就能和兩位教授面對面交流,還能接觸到來自全世界各地、數十位衰老生物學界大咖學者的研究成果、最新見解!

聲明 - 本文內容僅用於科普知識分享與抗衰資訊傳遞,不構成對任何產品、技術或觀點的推薦、背書或功效證明。文內提及效果僅指成分特性,非疾病治療功能。涉及健康、醫療、科技應用等相關內容僅供參考,醫療相關請尋求專業醫療機構並遵醫囑,本文不做任何醫療建議。如欲轉載本文,請與本公眾號聯繫授權與轉載規範。
參考文獻
[1] https://doi.org/10.1101/2025.06.26.661776
[2] Ma, S., & Gladyshev, V. N. (2017). Molecular signatures of longevity: Insights from cross-species comparative studies. Seminars in cell & developmental biology, 70, 190–203. https://doi.org/10.1016/j.semcdb.2017.08.007
[3] Tyshkovskiy, A., Bozaykut, P., Borodinova, A. A., Gerashchenko, M. V., Ables, G. P., Garratt, M., Khaitovich, P., Clish, C. B., Miller, R. A., & Gladyshev, V. N. (2019). Identification and Application of Gene Expression Signatures Associated with Lifespan Extension. Cell metabolism, 30(3), 573–593.e8. https://doi.org/10.1016/j.cmet.2019.06.018
[4] Liu, W., Zhu, P., Li, M., Li, Z., Yu, Y., Liu, G., Du, J., Wang, X., Yang, J., Tian, R., Seim, I., Kaya, A., Li, M., Li, M., Gladyshev, V. N., & Zhou, X. (2023). Large-scale across species transcriptomic analysis identifies genetic selection signatures associated with longevity in mammals. The EMBO journal, 42(17), e112740. https://doi.org/10.15252/embj.2022112740