半年營收增長48.02%,現金池仍在枯竭,榮昌生物“入不敷出”問題怎麼解?_風聞
医药研究社-44分钟前
拿下一筆總額超12億元的“license-out”後,榮昌生物及時交出了上半年的“成績單”。
財報顯示,今年上半年,該公司實現營業收入10.98億元,較去年同期增長48.02%;歸母淨利潤-4.50億元,上年同期為-7.81億元,同比減虧42.40%;扣非淨利潤-4.46億元,上年同期為-7.94億元,同比減虧43.88%。績後榮昌生物港股股價高開近4%。
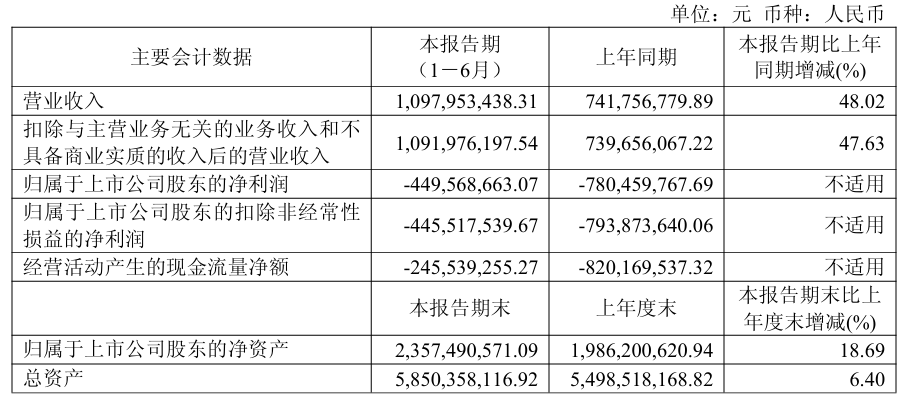 顯而易見,榮昌生物衝刺速度正持續加快,但是在抵達重要里程碑之際,虧損問題猶在、現金流吃緊,反映出公司身上包袱仍然比較沉重,增長步伐其實並不輕快。這種情況下,榮昌生物有什麼“解壓神器”?
顯而易見,榮昌生物衝刺速度正持續加快,但是在抵達重要里程碑之際,虧損問題猶在、現金流吃緊,反映出公司身上包袱仍然比較沉重,增長步伐其實並不輕快。這種情況下,榮昌生物有什麼“解壓神器”?
兩款商業化產品帶來增量
現階段,榮昌生物的核心驅動力顯然是商業化產品。
該公司財報顯示,上半年營業收入同比增加,就主要系泰它西普(商品名:泰愛®)和維迪西妥單抗(商品名:愛地希®)銷量及銷售額持續增加。
其中,泰它西普是公司自主研發的全球首款、同類首創(first-in-class)的注射用重組B淋巴細胞刺激因子(BLyS)/增殖誘導配體(APRIL)雙靶點的新型融合蛋白產品,可同時抑制BLyS和APRIL兩個細胞因子與B細胞表面受體的結合,“雙管齊下”阻止B細胞的異常分化和成熟,從而治療自身免疫性疾病。
 目前,泰它西普於國內獲批的適應症包括系統性紅斑狼瘡(SLE)、類風濕關節炎(RA)、重症肌無力(MG)等。
目前,泰它西普於國內獲批的適應症包括系統性紅斑狼瘡(SLE)、類風濕關節炎(RA)、重症肌無力(MG)等。
另一款核心產品維迪西妥單抗,是公司研發的中國首個原創抗體偶聯(ADC)藥物,也是我國首個獲得美國FDA、中國藥監局突破性療法雙重認定的ADC藥物。
據瞭解,該產品以腫瘤表面的HER2蛋白為靶點,能精準識別和殺傷腫瘤細胞,在治療胃癌(GC)、尿路上皮癌(UC)、乳腺癌(BC)等腫瘤的臨牀試驗中均取得了全球領先的臨牀數據;其用於治療胃癌、尿路上皮癌的新藥上市申請經優先審評審批程序,並作為具有突出臨牀價值的臨牀急需藥品分別於2021年6月、2021年12月在中國獲附條件批准上市。
自上述產品上市後,近年來榮昌生物集中火力加速商業推廣,構建增長基本盤。
財報就提到,截至2025年6月30日止,榮昌生物已組建約900人的自身免疫藥品銷售隊伍、超500人的腫瘤科藥品銷售隊伍,均分別完成超過1000家醫院的藥品准入。
值得一提的是,FIC藥物尤其是面向自身免疫、腫瘤等熱門賽道的首發產品本就佔據天然優勢,很容易通過醫保快車道以及積極的商業化佈局,釋放出不小增量。因此,泰它西普和維迪西妥單抗兩款產品撐起榮昌生物的業績,應該在市場的預期之中。
相比商業化產品帶來的實際效益,我們可能會更關注這背後榮昌生物支付了何種代價以及如何實現付出和回報的平衡。
增勢掩蓋不了資金壓力
榮昌生物的財務狀況雖明顯轉好,但算不上健康,“缺錢”問題仍然突出。
根據Wind數據,2022-2024年,榮昌生物淨虧損分別為9.99億元、15.11億元、14.68億元;經營現金流淨額分別為-12.60億元、-15.03億元、-11.14億元,上半年這一數據達-2.46億元,雖同比增加,但仍然為負。
另外,根據財報,榮昌生物上半年貨幣資金為12.74億元,短期借款則高達13.21億元,資產負債率達到59.70%,較去年同期增加6.01個百分點。
這背後,榮昌生物邁着“商業化+在研”的沉重步伐前進,各項成本着實難控。
財報顯示,隨着泰它西普和維迪西妥單抗的准入醫院數量及覆蓋藥房數量大幅度增加,上半年榮昌生物銷售費用為5.26億元,同比增長34.93%。
另一方面,公司也在有意識地減少研發費用,如2025年上半年這一指標已同比下降19.72%至6.47億元,但仍然處在高位,充分反映了多項研發佈局下控費空間並不大。
具體來看,目前榮昌生物共有六個分子處於臨牀開發階段,覆蓋幾十種適應症。
針對商業化產品,公司正在拓展應用維度,如推進泰它西普用於治療原發性乾燥綜合症(pSS)、免疫球蛋白A腎病(IgAN),探索維迪西妥單抗聯合治療HER2表達UC的各類臨牀應用的可能性等。同時發現並研究新靶點或新作用機制,RC28、RC88、RC148、RC278、RC288等在研管線就承載了榮昌生物的擴張野心。
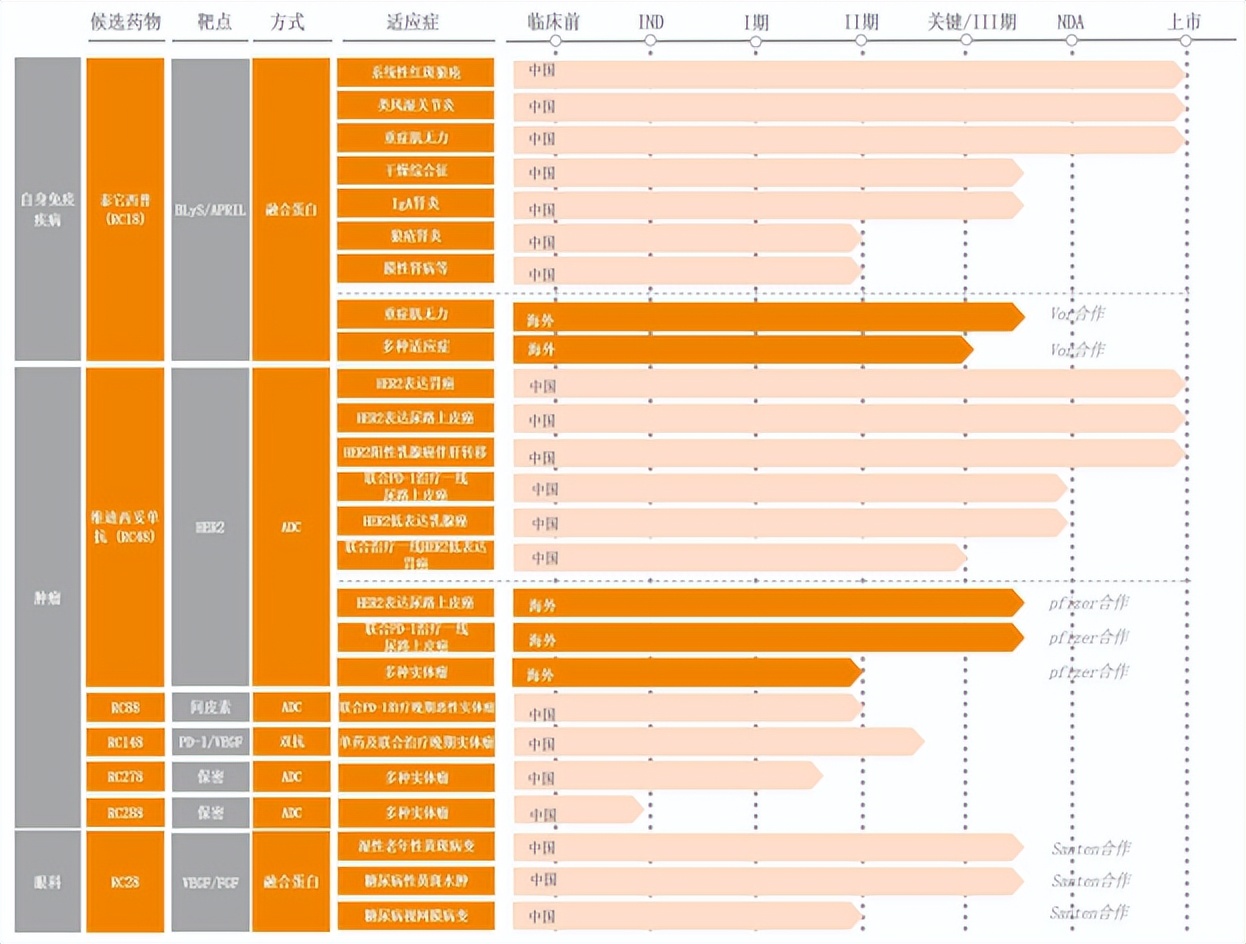 而與之對應的就是僅兩款產品上市,貢獻的商業化增量顯然難以覆蓋各項支出。這種情況下,榮昌生物仍然剛需“輸血”。
而與之對應的就是僅兩款產品上市,貢獻的商業化增量顯然難以覆蓋各項支出。這種情況下,榮昌生物仍然剛需“輸血”。
榮昌生物的“解壓神器”
首先募資是必要的。
公開資料顯示,在2024年3月,榮昌生物推出25.5億元A股定增預案,然而這一融資計劃落地困難,公司後於2024年7月將定增募資額下調至19.53億元,但截至目前這筆融資也未完成。
另外,此前榮昌生物公告稱,公司已於2025年5月29日按配售價每股配售股份42.44港元的價格,向不少於六名承配人成功配發及發行合共1900萬股新H股,佔經配發及發行配售股份擴大後的已發行H股總數約9.11%,以及已發行股份總數約3.37%;公司將收取的配售事項所得款項淨額(經扣除配售事項的佣金及估計開支後)合計約為7.96億港元。
這些資金利於緩解榮昌生物的短期運營壓力,但顯然難填長期創新藥開發的“無底洞”。於榮昌生物而言,要實現可持續的經營,還需要BD等手段來撬動在研管線的潛在價值。
今年,榮昌生物就推進了好幾筆重磅BD。比如,2025年6月,該公司將具有自主知識產權的泰它西普有償許可給Vor Bio,Vor Bio將獲得在除大中華區以外的全球範圍內開發和商業化的獨家權利。
作為對外許可交易對價一部分,榮昌生物及其全資附屬主體榮普合夥將從Vor Bio取得價值1.25億美元現金及認股權證,最高可達41.05億美元的臨牀註冊及商業化里程碑付款,以及高個位數至雙位數銷售提成款。於2025年7月14日,公司已收到由Vor Bio支付的4500萬美元首付款。
今年8月,榮昌生物發佈公告稱,擬將自主研發的眼科創新藥RC28-E在大中華區及韓國、泰國、越南、新加坡、菲律賓、印度尼西亞及馬來西亞的獨家開發、生產和商業化權利,有償許可給日本參天製藥株式會社在華子公司。
根據協議,榮昌生物將取得2.5億元人民幣的不可退還且不可抵扣的首付款,以及最高可達5.2億元人民幣的開發及監管里程碑付款和最高可達5.25億元人民幣的銷售里程碑付款。此外,榮昌生物還將根據授權地區的產品銷售額收取高個位數至雙位數百分比的梯度銷售分成。這筆交易正是文章開頭提到的超12億元“license-out”。
至此,榮昌生物的重要“輸血”路徑已經較為清晰,不過效果有多大尚未可知。尤其是BD,雖然利於公司實現從“外部輸血”到“自我造血”,但其中變數較大,常受到合作伙伴發展狀態、市場競爭等諸多因素影響。
據悉,Vor Bio近年經營情況不佳。今年5月8日,Vor Bio宣佈暫停所有臨牀和生產活動,裁員約95%,僅保留8名員工以維持基本運營並尋求戰略替代方案。
而榮昌生物與參天製藥的交易中,RC28-E這款產品的競爭力也在影響市場預期。
公開資料顯示,RC28-E是全球首個VEGF/FGF雙靶點融合蛋白藥物,可用於治療濕性年齡相關性黃斑變性(wAMD)、糖尿病性黃斑水腫(DME)等,目前處於三期臨牀階段,計劃明年下半年在中國申報上市,主打雙靶點、長效化等差異化優勢。而現階段類似藥物正在不斷湧現,拜耳、羅氏、諾華等跨國巨頭都是強有力競爭者。
或許也是基於這些因素,榮昌生物這兩起BD並未在二級市場掀起太大波瀾。對外授權參天製藥的消息傳出當天,榮昌生物A股上漲1.66%,港股上漲1.18%。
來源:醫藥研究社