國內首款可使甲亢突眼回退藥物上市,信達生物IGF-1R靶向藥信必敏獲批
王力邮箱:[email protected]
【文/王力 編輯/周遠方】
3月14日,國家藥品監督管理局管網顯示,信達生物(01801.HK)研發的替妥尤單抗N01注射液(商品名"信必敏")獲得上市批准,該藥物作為中國首個、全球第二款IGF-1R靶向抗體藥物,獲批適應症為甲狀腺眼病(Thyroid Eye Disease, TED)。
甲狀腺眼病是一種與甲狀腺問題緊密相關的器官特異性自身免疫疾病,是成人眼眶疾病中最常見的類型,特別是在40至60歲的人羣中發病率較高。據估計,該病的年發病率大約為每10萬人中有16名女性和2.9名男性患者,患病率在0.1%到0.3%之間。值得注意的是,近年來甲狀腺眼病的發病年齡有下降的趨勢。該病會導致眼球突出和複視等症狀,嚴重時甚至可能引起失明,對患者的視力和整體生活質量造成重大影響。
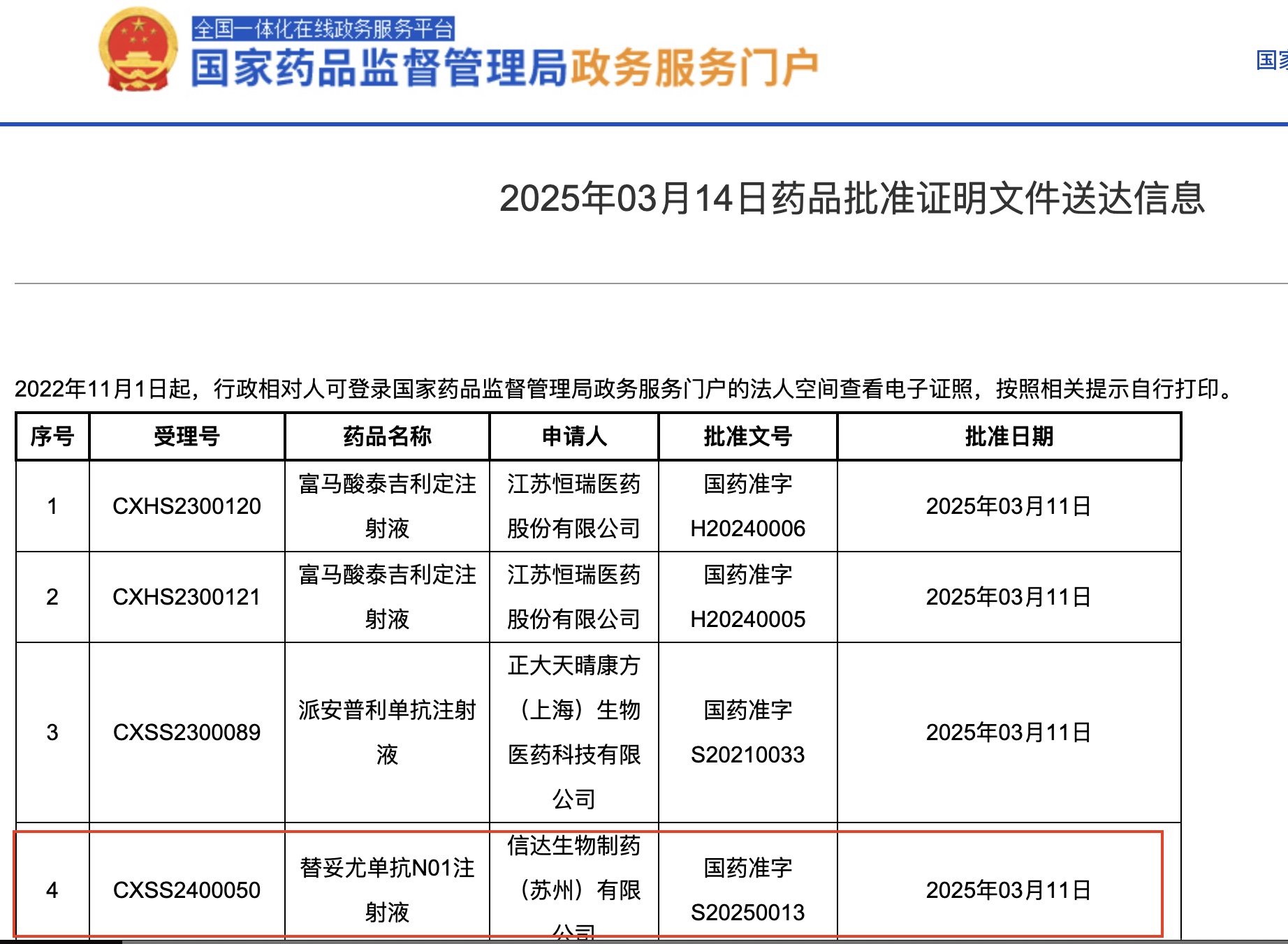
截圖來自國家藥監局
目前,臨牀治療主要依賴於糖皮質激素,但其副作用如繼發性骨質疏鬆等較為顯著。突眼症狀的改善並不理想,並且存在與激素相關的全身性副作用。二線治療方案包括再次使用激素衝擊療法、聯合眼眶放療或使用其他免疫調節劑,但治療效果往往不盡人意。近期,國內外的多項臨牀治療指南和專家共識已將靶向IGF-1R的生物製劑作為甲狀腺眼病二線治療的推薦方案,特別是對於那些伴有明顯突眼或複視的患者,靶向IGF-1R的生物製劑可作為首選治療。
中國工程院院士、上海交通大學醫學院附屬第九人民醫院眼科的範先羣教授指出:“作為眼科醫生,我特別高興地看到中國首個甲狀腺眼病新藥——替妥尤單抗N01獲批上市。我相信它將為中國患者提供與國際接軌的治療方案,並期待它能為全球甲狀腺眼病患者帶來更多的治療選擇。”
在競爭格局方面,美國安進公已被很多美國患者使用。但Tepezza療程費用約300萬元的價格壁壘,導致國內患者可及性極低。信必敏的治療費用僅為1/15。並且由於該藥物給藥劑量與體重相關,中國患者體重較美國患者更輕,實際治療費用也將更低。
除價格外,信必敏的臨牀效果也優於Tepezza。2024年,該藥物在中國甲狀腺眼病受試者中開展的3期註冊臨牀研究達成主要終點,與Tepezza臨牀數據相當甚至更優。臨牀數據顯示,採用信必敏治療24周時,患者突眼回退≥2mm的應答率高達85.8%,炎症和複視等症狀也顯著改善。
從企業戰略佈局觀察,信達生物此次突破意味着其正式切入眼科及內分泌千億級市場。作為國內PD-1單抗領域的頭部企業,除已獲批上市的15款藥,信達生物目前還有3個品種在國家藥品監督管理局上市審評中,3個新藥分子進入III期或關鍵性臨牀研究,另有16個新藥品種已進入臨牀研究。
從產業政策維度觀察,此次獲批恰逢《“十四五"生物經濟發展規劃》實施關鍵期,政策對創新藥"全球新"靶點的支持力度持續加大。信必敏作為具備國際競爭力的改良型生物藥,其商業化表現或將成為檢驗我國醫藥創新成果轉化效率的重要樣本。
信達生物臨牀開發高級副總裁錢鐳博士表示:“面向未來,信達生物將持續深耕腫瘤、自身免疫、代謝及心血管、眼科四大治療領域,陸續推出更多高質量的生物創新藥。”
本文系觀察者網獨家稿件,未經授權,不得轉載。