譚驍天| 一滴血的秘密:美國公司的騙局之後,我們能做什麼
guancha
【文/ 譚驍天】
一滴血裏面有什麼?從一滴血裏又能看到什麼?
因為美國公司的科技騙局,人們曾經對“一滴血診斷”失去了信心。但是現在,在我們研製的“尖端”系統裏,一滴血裏包含着的海量信息都能方便獲取,也許將改變疾病檢測的未來。
“一滴血測200種病”的騙局是怎麼回事
2018年,《Bad Blood》一書橫空出世,講述了Theranos公司“一滴血測200種病”的神話崛起與崩塌,引發了全球對“微量血液檢測”的深度反思。這場科技泡沫的主角,是被稱為“女版喬布斯”的伊麗莎白·霍姆斯(Elizabeth Holmes,ps:這個姓其實就是福爾摩斯的另一種譯法)。
2003年,這位被貼上“天才少女”標籤的創業者19歲,她從斯坦福輟學,創辦了Theranos公司,立志用“一滴血”顛覆整個醫療行業。她總穿着一件與喬布斯同款的黑色高領毛衣,經常用低沉而富有磁性的聲音向投資人描繪一個充滿誘惑的未來:
“只需從指尖輕輕一紮,採集一滴血(約50微升,相當於一滴水),放入Theranos精心設計的微型採血管Nanotainer,再插進一種名為Edison的神秘設備中,便可檢測200多種與疾病有關的分子指標——從血糖、膽固醇到腫瘤標誌物。這種方式無痛、快捷,還能大幅節省醫療成本。更重要的是,由於無需採集靜脈血,用户甚至可以在藥店、甚至居家自行完成採樣。”

Theranos公司的創始人霍姆斯曾提出使用指尖血檢測二百餘種疾病標誌分子 左圖來源: every-day-development.com,右圖來源usatoday.com
在她的構想中,Theranos將開發出一整套可適配10–50微升血樣的檢測技術。除了血常規分析(目前已廣泛應用),她還希望實現對代謝物、激素、酶、腫瘤標誌物等分子指標的檢測。
而其中最具挑戰的,就是那些本身在血液中含量極低(通常在皮摩爾級,十億分之一毫摩爾)的分子,比如早期癌症相關的蛋白標誌物。這類指標必須通過抗體等高特異性的免疫探針和配套的高靈敏度生物傳感系統(如磁珠等)進行分析,技術門檻極高。如果在2010年前後就能用10微升指尖血完成這類複雜檢測,無疑將是一次革命性的突破。但也正是因為目標如此高遠,實現的難度也同樣很高。
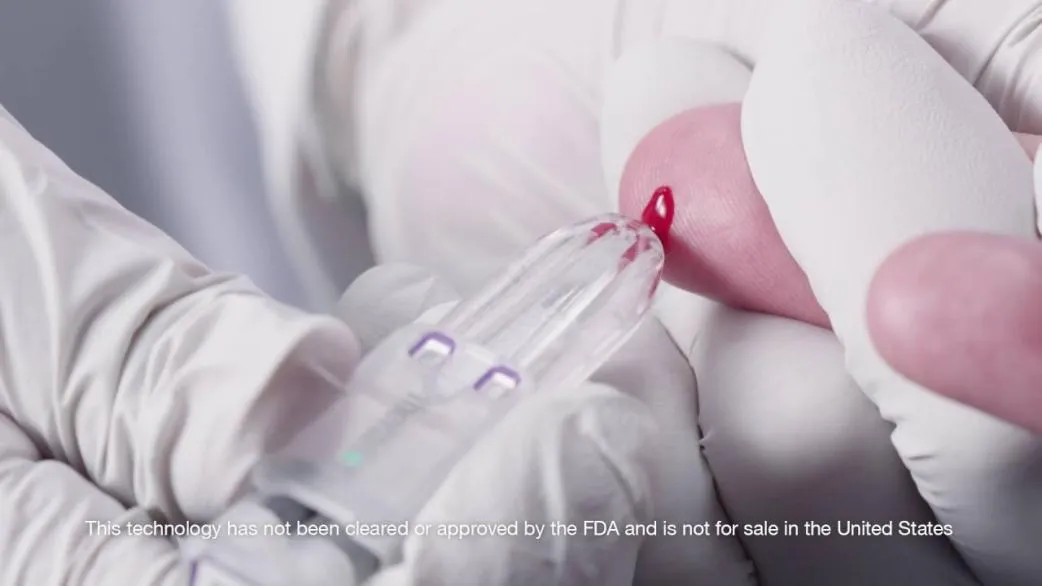
Theranos公司開發的微量指尖血採集裝置,後端配有適配微量樣本的真空集血管 Theranos公司宣傳片
Theranos團隊很快發佈了一款便捷易用的指尖血採集裝置,還附帶有能定量保存50微升微體積血液樣本的抗凝管。由於有了實物加持,這個充滿未來感的設想迅速引來各路名人投資:拜登、基辛格、切尼、默多克等紛紛站台支持,Theranos估值一度飆升至90億美元。
然而,他們遲遲未能真正突破微量樣本免疫分析方面的技術難題,現實與承諾之間的差距越來越大。那個名為 “Edison” 的分析設備,本質上和傳統的磁珠化學發光平台並無本質區別,只是試圖將操作體積縮小到微升級別。但這反而讓技術難度陡然上升,設備頻頻出現取樣不穩、數據不準的問題,尤其是在面對低濃度標誌物檢測時,幾乎無法完成原定任務。
為了維持運營,Theranos的實驗室只能大量依賴傳統大型檢測設備“兜底”分析。問題是,這類檢測平台本身設計是用於更大體積的樣品,名義上需要100–200微升樣品,但實際操作常需300–500微升,遠超指尖血所能提供的體積。如果一定要進行測試,只能對指尖血樣本進行高倍數的稀釋。因為老闆霍姆斯堅持使用微量指尖血進行一百餘項免疫分析,技術人員不得不將原本僅有的20–50微升指尖血血清反覆稀釋,有時甚至會被稀釋上百倍,才能滿足傳統免疫分析設備的樣本量要求。

因進樣裝置限制,常規免疫檢測設備需要的樣本體積較大,無法分析指尖血這樣的微小體積樣本 作者自制
在嚴重偏離規範的前提下,檢測結果的準確性幾乎無法保證:同一位患者,前後兩次結果可能天差地別——一次“完全正常”,另一次卻提示“高度癌症風險”。到了後期,Theranos的整個運作方式,已幾乎與詐騙或傳銷無異。
然而,泡沫總是有破滅的那一天。2015年至2018年間,《華爾街日報》的調查記者約翰·卡雷魯持續追蹤報道,最終戳破了這個被精心包裝的技術神話。隨着騙局曝光,Theranos轟然倒塌。2018年公司徹底關閉,霍姆斯因多項欺詐罪被判入獄11年。
要知道一滴血裏有什麼,需要真正適配的傳感技術
Theranos倒下之後,“一滴血診斷 ”這一原本充滿未來感的概念也彷彿被打入冷宮。Theranos開發的微型採血器件也從此消失在歷史長河中,哪怕它本身其實是一個設計精巧、採樣便捷的工具。更諷刺的是,在相當長一段時間裏,甚至連生物傳感領域內也少有人再敢高調談論用指尖血進行腫瘤等重大疾病的篩查——哪怕這個想法本身並不荒唐。
Theranos的失敗,並非因為“一滴血”不是一種有效樣本,而是因為如果要分析好這滴血,首先需要開發一整套複雜的傳感分析機制、樣本處理方法、配套傳感、反應器件及設備。他們開了個好頭,但沒能真正解決這個問題。Theranos的教訓也告訴我們,僅靠概念無法解決科學問題,要真正瞭解一滴血的潛力,需要回到科學本身。
如果我們願意回到科學的基本面,做一做簡單的計算,看看“一滴指尖血”中到底藏着什麼,就會發現:僅僅50微升的血液中,就包含着約2.5億個紅細胞、35萬個白細胞和上千萬個血小板,這個數量已經非常可觀了!由於相對龐大的數量和相對較為明顯的形態、尺寸差異,目前通過指尖血進行外周血細胞的分類和計數已經不再是什麼難事。讀者朋友去醫院做快速血常規檢查,用的就是基於指尖血的測試。
但是,指尖血承載的更深層次的生物分子信息仍像一團難解的迷霧。特別是免疫功能的分析,相比之下要比單純看細胞數量要複雜不少。仍以50微升指尖血為例,其中一般包含着5到15萬個淋巴細胞,尤其是T細胞(3-10萬個左右)和B細胞(1萬個左右),它們正是識別病原、清除感染、建立免疫記憶的核心力量。B細胞可以分泌抗體,而T細胞可以釋放細胞因子調節免疫應答,也可以直接殺傷靶細胞。
每一次感染病毒或細菌,或者接種疫苗,人體都會產生針對該特定病原體的獨特抗體譜(免疫響應指紋)。而即便只有一微升血液,其中也可能含有十萬到上百萬個特異性抗體分子,以及數萬個調控免疫的細胞因子。這些微量卻信息豐富的分子,悄然記錄着個體的疫苗接種史、感染經歷、當前免疫及疾病狀態——不僅能回答“是否曾經感染過”,更能揭示“現在還有沒有免疫保護”。然而,即便是樣本中含有數十萬個目標抗體,在基於一滴血的免疫功能的分析方面,磁珠化學發光等傳統大體積方法常常是愛莫能助。
我們難以從一滴血中讀出足夠信息,原因並不是其生物信息含量不足,而在於缺乏與之匹配的檢測手段和技術路徑。這也正是我和我的團隊試圖去改變的方向。
我們設計了一個“尖端”系統
讓我們盤點下經典的免疫防護能力分析技術,要精準評估抗體免疫功能和T細胞免疫響應能力,傳統的方法有ELISA、病毒中和實驗、干擾素釋放試驗等免疫檢測手段。
這些成熟的方案,全流程極為漫長。特別是病毒中和實驗,常需要將細胞、病毒、血清樣本在高防護性的特殊實驗室中共同培養兩到三天,不僅很慢,而且所需的人力、耗材成本同樣高昂。更為重要的是,上述傳統方法在微量樣本面前往往“失效”——樣本量不夠,稀釋又會導致信號太弱。針對T細胞功能的干擾素釋放試驗也有類似的問題。
為了破解微量血樣檢測的技術瓶頸,我們開發了一套全新的便攜式化學發光免疫分析平台,它從一開始就是為“只用一滴血”而設計的,目標很明確:只用1微升指尖血,就能快速得出結果。平台包含可與移液槍頭一體化集成的微流控免疫反應器及一個化學發光成像站,總重量大約為3kg, 一名成年男性用一側手臂可以輕鬆拿起,這套系統名叫TOI(Tip Optofluidic Immunoassay),我們組裏的小夥伴還給它起了個小名,叫做“尖端”。
在免疫分析元件方面,我們採用工業級微注塑工藝,打造出一種可直接裝在移液槍頭上的微流控反應器。它本質上是一根精細的毛細管,通道窄、體積小,但每微升液體的管壁接觸面積極大,有效提高了內壁與蛋白分子的吸附能力強,顯著縮短了分子擴散距離。不僅縮小了抗體用量,也讓抗體和抗原能更快“遇上”。整個免疫吸附反應幾分鐘內即可完成。
配合高靈敏度的CMOS相機和經過精心優化的緩衝液體系,即使是pg/mL級別的低丰度蛋白也能被準確捕捉。最終,TOI平台實現了傳統方法難以同時達成的檢測性能:1–15微升血樣、40分鐘內同步完成結合抗體水平與中和能力的評估,極限信噪比可達10000,動態範圍覆蓋4個數量級。

(A)便攜式化學發光免疫分析平台(B)可與常規移液槍頭集成的微流控免疫反應器件“尖端” 作者自制
在抗體檢測方面,TOI不僅能判斷體內有沒有抗體,還能進一步評估這些抗體有沒有“戰鬥力”。
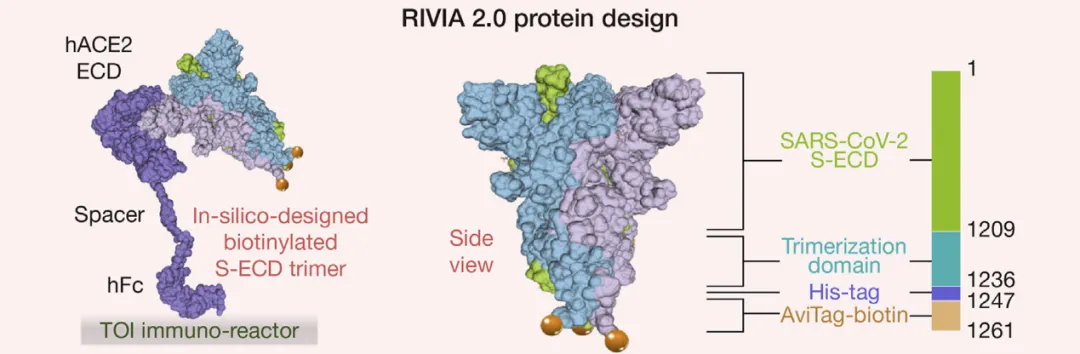
為了實現抗體中和能力的體外分析,我們還通過合成生物學的方法設計了一組蛋白探針 作者自制,已發表在hLife
為了解決傳統病毒中和試驗漫長且費力的困擾,我們開發了一套在TOI平台上直接使用重組蛋白進行中和能力測試的純體外評估體系。我們設計了一套更安全、更方便、更穩定的蛋白探針組合,用來模擬病毒和人體細胞結合的關鍵過程。其中包括一個可與傳感器定向結合的重組細胞表面受體,還包括一個用來“偽裝”成病毒的刺突蛋白三聚體探針(探針尾部還有一個能引發化學發光的“信號標籤”)。
在實際測試中,如果血液中含有具備中和能力的抗體,就會阻止這兩種探針結合,導致發光信號下降。得益於我們對探針結構和反應空間的優化,TOI抗體分析的靈敏度比傳統假病毒實驗大幅提高。配合我們開發的結合抗體定量方法,只需一小滴血,就能同時判斷疾病特異性抗體的數量和功能。雖然技術方案上比較“激進”,但整套流程快速、準確,為個體免疫狀態的即時評估提供了真正可落地的技術方案。
在這一系列研究中,包括蛋白分子探針、免疫反應器、化學發光觀測系統在內的整套TOI系統,全部的設計、開發、配件生產工作均在國內完成。在微流控免疫功能分析這個小領域裏,雖然尚未實現整個供應鏈100%國產,但最起已經沒有了被卡脖子的後顧之憂。
走進真實世界,“尖端”能告訴我們很多信息
採集志願者指尖血 作者自制,已發表在hLife
2023-2024年,我們以“請志願者喝一杯奶茶”為吸引,招募了身邊的科研戰友和熱心羣眾志願者。靠着他們捐出的一滴滴指尖血,我們得以一窺人體免疫系統對傳染性病原體的反應。原本我們只是想驗證“能不能測得出”,沒想到結果遠超預期——這滴血還真能測出不少有趣的東西。
1. 體內抗體的能力
我們檢測了志願者體內針對新冠病毒的抗體。
首先,我們發現,疫苗怎麼打,真的很重要。那些接種過“滅活疫苗+重組蛋白或mRNA疫苗”組合方案的志願者,抗體水平往往比只接種滅活疫苗的更高,而且更能中和病毒。換句話説,同樣是打了疫苗,混搭一下更強,比只打一種疫苗的要“扛打”得多。
其次,我們還觀察到,在多次感染後,免疫系統不是一成不變地重複過去的應答,而是在不斷調整、更新自己的“識別檔案”,逐漸適應與病毒的戰鬥。
更有意思的是,我們還觀察到一個非常實際的趨勢:抗體水平與未來感染風險之間,存在明確的“預警關係”。一旦抗體濃度低於某個閾值,該個體在接下來的六個月裏就更容易“中招”。這個規律為精準健康管理和個體風險預測提供了切實可用的參考。
在眾多志願者中,我們還遇到了幾位“骨骼清奇的高手”,他們血液中的抗體對多個變異毒株都能高效結合,併產生強力中和反應,堪稱“常勝將軍”。從科研的角度看,這樣的人羣特別有研究價值,因為他們體內的抗體或記憶B細胞,可能正是未來開發廣譜抗體藥物或疫苗的關鍵線索。換句話説,説不定以後抗病毒的“秘密武器”,就藏在他們當初留給我們的那一滴血裏。
2. T細胞的能力
當然,抗體只是免疫系統的一部分。真正決定一個人能否長期保持免疫防護的,是T細胞的記憶能力。它們不像抗體那樣第一時間出擊,更像是訓練有素的預備隊,在身體再次遇到病原時,能快速響應,發動後續免疫攻勢。
以結核病為例,它就是一類高度依賴T細胞免疫反應進行臨牀診斷的傳染病。但傳統的T細胞響應檢測方法,比如干擾素釋放試驗(IGRA),需要抽3到5毫升靜脈血、培養近一天,檢測流程長、門檻也高,不太適合做現場篩查或大規模推廣。所以我們就在TOI平台的基礎上,把“微量血樣”的思路進一步應用到了T細胞功能檢測上。最終開發出了CM-IGRA(Consolidated Microscale Interferon-γ Release Assay)。
它延續了TOI的設計理念,只需少量血液裏的少量T細胞,就可以判斷特異性T細胞在遇到結核抗原刺激時,是否還能分泌干擾素γ——也就是測它們的“免疫細胞是否還記得結核抗原”。根據目前的測試結果,其與醫院傳統IGRA的一致率達到了98%。這套系統特別適合在流動人羣密集、資源有限的基層地區使用。
目前我們已經開始嘗試用真正的指尖血樣本,來做多種病原的T細胞免疫分析,也取得了不錯的早期結果。我們還發現T細胞免疫響應與抗體免疫響應存在着一定的互補性,希望能在今後的實驗中得到更為明確的解釋。
結語
目前,我們也正在拓展TOI與CM-IGRA的適應範圍,比如嘗試更方便、更穩定的指尖血保存方案,也比如探索如何利用一滴血,同時檢測多種病原相關的抗體丰度、中和能力與T細胞響應能力。這一組合不僅適用於個體風險評估,還可為流行病學調查、羣體免疫監測與疫苗接種策略的制定提供精準依據。
Theranos的崩塌,曾讓“一滴血”成為科研圈諱莫如深的詞彙。但讓它失敗的,不是這個概念本身,而是把沒準備好的技術包裝成包打天下的神話。如今,隨着微流控、生物傳感、合成生物學和人工智能等多項技術的交匯融合,我們終於有能力重新審視這滴血——並真正聽懂它想傳遞的信息。
一滴血中包含的生物信息未必能有效診斷所有疾病,但經過我們看似“離經叛道”的嘗試,我們證明了基於指尖血的免疫分析測試足以捕捉免疫系統的關鍵狀態與功能。這不僅為傳染病的精準防控帶來了新的可能,也為疫苗評估、個體健康管理、重大疾病篩查等領域開闢了快速、便捷的解決路徑。
這不是一場靠故事推動的幻想,而是一次以技術為根基的現實躍遷。“一滴血”不該是離譜騙局的代名詞,它是科學可以抵達的目標。悄然之間,“未來”已來。

參考文獻:
[1] Tan X, Chai Y, Li R, et al. 1 μL, 40min: Multimodal COVID-19 antibody protection evaluation with tip optofluidic immunoassay[J]. hLife, 2025.
[2] Zhang B, Xu Y, Huang Z, et al. Consolidated Microscale Interferon-γ Release Assay with Tip Optofluidic Immunoassay for Dynamic Parallel Diagnosis of Tuberculosis Infection[J]. Anal. Chem., 2025, 97 (5), 2863–2872.
[3] Lyu Y, Zhang B, Chai Y, et al. A Quantitative First Passage Time Model for Tubular Microfluidic Immunoassays[J]. ACS Sens., 2025, 10 (2), 1387–1397.
本文出品自“科學大院”公眾號(kexuedayuan)
科學大院是中國科學院官方科普微平台,致力於最新科研成果的深度解讀社會熱點事件的科學發聲
主辦機構:中國科學院學部工作局
運行機構:中國科學院計算機網絡信息中心
技術支持:中國科普博覽
