泰諾心癌風險數據被製造商葛蘭素史克保密了40年 - 彭博報道
Anna Edney, Susan Berfield, Jef Feeley
 插圖:Ibrahim Rayintakath for Bloomberg Businessweek
插圖:Ibrahim Rayintakath for Bloomberg Businessweek
這家小型英國公司有時被稱為格拉克索大學,因為它進行重要的製藥研究,但很少能開發出盈利藥物。然後,格拉克索實驗室的科學家們創造了一種他們稱之為雷尼替丁的分子,並於1978年獲得了美國專利。這種分子是新的,但並非新穎。科學家們有時會尋找一種方法來模仿一種已經成功的藥物,就像這種可以治癒潰瘍並可用於治療胃灼熱的藥物一樣。他們迅速開發了雷尼替丁,並且美國食品藥品監督管理局也迅速審查了它。格拉克索給它取名為贊特克。
格拉克索將其推廣為比啓示它的藥物——泰力美更好、更安全,並不久之後,贊特克超越了泰力美,成為世界上最暢銷的處方藥。多年來,格拉克索幾乎依賴贊特克實現了近一半的銷售額和幾乎相同的利潤。該公司獲得了伊麗莎白女王頒發的獎項;首席執行官被封為爵士。贊特克創造了聲譽和財富。它為現代格拉克索提供了資金,經過合併、收購和分拆後,最終成為了 GSK Plc,一家現在價值約730億美元的公司。其最受歡迎的藥物包括抗抑鬱藥帕羅西汀和威爾布特林,以及帶狀皰疹疫苗希格瑞克斯。
但贊特克除外。2019年,發現這種藥物受到可能致癌物質的污染。這不是偶然或是少數批次的錯誤。毒素是由雷尼替丁本身產生的。贊特克的生產商和全球各地的衞生監管機構召回了這種藥物,到2020年春季,美國食品藥品監督管理局強制將其從市場上撤下。沒有公司能夠生產它;沒有人應該攝入它。這種致癌物質被稱為NDMA,曾被添加到火箭燃料中,現在僅用於誘發實驗室老鼠的癌症。美國食品藥品監督管理局表示,攝入微量不會有害。但檢測結果顯示雷尼替丁中NDMA的含量過高,並且隨着時間的推移還會產生更多。沒有一種版本看起來是安全的。
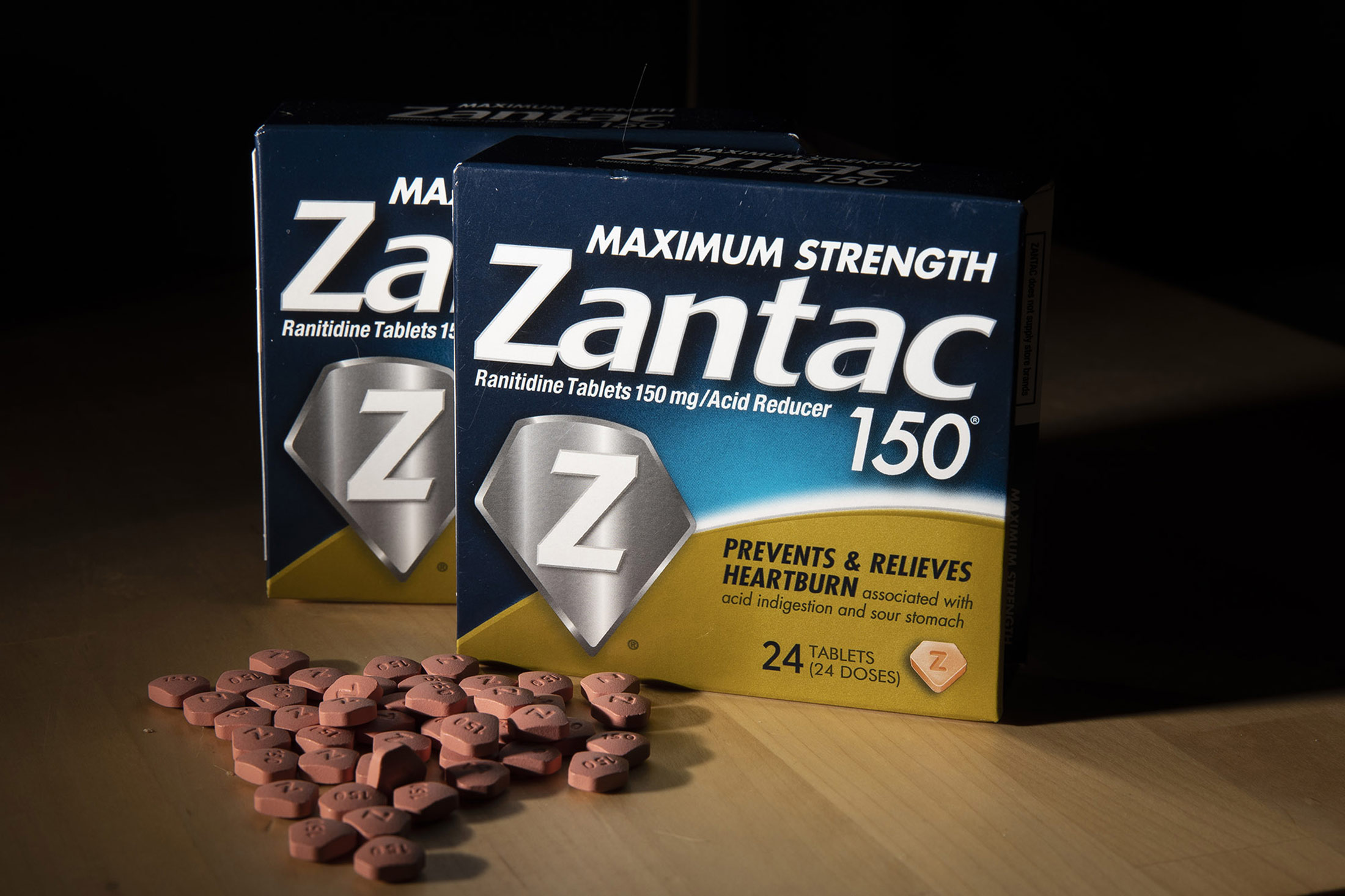 超過70,000人服用贊他安和其仿製藥的人正在起訴葛蘭素史克公司。攝影師:Drew Angerer/Getty Images從雷尼替丁問世到終結,葛蘭素史克公司的科學家和獨立研究人員一直在警告其潛在危險。數以百計的文件、成千上萬頁的資料揭示了這四十年的歷程,其中許多從未公開。 彭博商業週刊審查了法庭文件,其中許多仍然保密,以及通過信息自由法案請求獲得的研究、FDA記錄和新藥申請。它們顯示FDA在批准雷尼替丁時考慮了癌症風險。但葛蘭素史克沒有分享一項關鍵研究。多年來,該公司還支持了旨在減輕擔憂的有缺陷的研究,並選擇不定期運輸和儲存藥物,這可能緩解了問題。葛蘭素史克銷售了一種可能會傷害人的藥物,試圖貶低這一證據,並從未給任何人最小的警告。
超過70,000人服用贊他安和其仿製藥的人正在起訴葛蘭素史克公司。攝影師:Drew Angerer/Getty Images從雷尼替丁問世到終結,葛蘭素史克公司的科學家和獨立研究人員一直在警告其潛在危險。數以百計的文件、成千上萬頁的資料揭示了這四十年的歷程,其中許多從未公開。 彭博商業週刊審查了法庭文件,其中許多仍然保密,以及通過信息自由法案請求獲得的研究、FDA記錄和新藥申請。它們顯示FDA在批准雷尼替丁時考慮了癌症風險。但葛蘭素史克沒有分享一項關鍵研究。多年來,該公司還支持了旨在減輕擔憂的有缺陷的研究,並選擇不定期運輸和儲存藥物,這可能緩解了問題。葛蘭素史克銷售了一種可能會傷害人的藥物,試圖貶低這一證據,並從未給任何人最小的警告。
超過70,000人服用贊他安或其仿製藥的人正在美國州法院起訴該公司出售一種可能被污染和危險的藥物。這些訴訟中的第一起預計將於2月底在加利福尼亞州阿拉米達縣的加利福尼亞高級法院開始,但可能會推遲到夏季以適應法官的時間安排。其他在後來幾年銷售贊他安的公司,包括輝瑞公司和賽諾菲,也被訴訟涉及。
不到一毫克的NDMA就能使小鼠細胞發生突變。兩克NDMA可以在幾天內殺死一個人
去年12月,GSK在聯邦法院的另一組案件中贏得了有利的裁決。美國佛羅里達州南區地方法院法官羅賓·羅森伯格(Robin Rosenberg) 駁回了成千上萬起聯邦訴訟,這些案件曾在她的法庭上合併進行預審程序。她宣佈,“科學界沒有普遍接受關於雷尼替丁和癌症之間存在可觀察的、統計學上顯著的關聯。” GSK認為羅森伯格的看法是對這些主張的最終結論。該公司發言人凱瑟琳·奎因(Kathleen Quinn)在一份聲明中表示:“法院的觀點與GSK和其他共同被告在整個訴訟過程中一直持有的立場一致。”“經過三年多的廣泛研究,包括對13項關於雷尼替丁使用人類數據的同行評議流行病學研究,科學共識是,沒有一致或可靠的證據表明Zantac(雷尼替丁)增加任何類型癌症的風險。”代表提起訴訟的律師們計劃上訴。
GSK仍然必須應對等待在州法院的數萬起案件,那裏的法官不受聯邦法院裁決的約束。該公司在一份聲明中表示,“將繼續積極捍衞自己,包括反擊此訴訟中的所有主張。” GSK拒絕進一步置評。
每個公共衞生機構,從環境保護局到FDA再到世界衞生組織,都表示NDMA可能會導致人類患癌症。但要證明某個特定人的癌細胞是由某家公司的藥物突變引起的是複雜的。Glaxo的決定表明它從未想過考慮這種可能性。線索是存在的。文件顯示Glaxo更傾向於不去發現它們。
原告律師: 在Zantac上市近50年的任何時候,Glaxo是否導致任何人檢測其向美國消費者銷售的產品Zantac中可能的人類致癌物NDMA的存在?
Glaxo高級醫療顧問: 據我所知沒有。
—證詞,2021年6月
NDMA,即N-亞硝基二甲胺,是一種可溶於水的黃色液體。它沒有氣味,也沒有太多的味道。它首次被與癌症聯繫起來是在1956年,對肝臟最具毒性。它是一類被稱為亞硝胺的化學物質之一,到了1970年代被認為是迄今發現的最強致癌物質。它在被測試的每個動物物種中都會引發癌症。少於一毫克的NDMA單劑量就能突變小鼠細胞並刺激腫瘤生長,2克就能在幾天內殺死一個人。
William Lijinsky在1969年擔任美國政府的癌症研究員時確定了亞硝胺可以在胃中形成。亞硝酸鹽是一種常見的化學物質,存在於醃製和烤肉、啤酒、咖啡和蔬菜中,它可以與另一類化學物質——胺類化合物結合,這些化合物存在於許多藥物中。胃酸創造了理想的反應環境。一次產生的亞硝胺量可能微不足道,但隨着時間的推移可能會變得危險。Lijinsky發表了關於亞硝胺的研究。他在國會作證。他認為最簡單的減少問題的方法是限制食品製造商可以添加的亞硝酸鈉以保鮮和調味肉類的量。火腿、培根、燻牛肉、醃牛肉、香腸:原來是常見引起胃灼熱和反流的食物。
他還評估了不同的胺類化合物,總共有幾百種,看看它們中哪些在模擬胃酸條件下能夠形成亞硝胺。它們全都能。當時還不存在雷尼替丁,但它也包含胺基結構。利金斯基的研究在1979年導致一種常用作鎮靜劑的抗組胺藥物被從市場上下架,因為它有潛在致癌風險。
羅莎莉·利金斯基是一位遺傳毒理學家,最近從FDA退休,她與丈夫一起研究了亞硝胺。她説:“他認為它們是最重要的致癌物質。” 但他失去了聯邦資助用於他的研究,她説,這在很大程度上是因為來自食品和製藥行業的壓力。他在2004年因中風去世,認為自己的工作沒有用處。
我認為監管機構在亞硝酸鹽和亞硝胺問題上的行動不夠積極。如果他們願意尋找,已經有大量信息可供獲取。當然,製造公司對任何變化都存在巨大的反對。
—威廉·利金斯基,1977年國會證詞
1980年11月,一家知名英國投資公司的著名製藥分析師向投資者發佈了一份名為“葛蘭素史克,雷尼替丁——令人擔憂”的報告。葛蘭素史克正準備向FDA申請在美國銷售雷尼替丁。分析師寫道,美國的學術研究表明,在胃部的某些特定條件下,雷尼替丁可能會形成一種潛在危險的化合物。這些條件就是利金斯基和其他人描述的化學反應;產物是一種可能導致癌症的化學物質。令人擔憂的是:對銷售的可能影響。分析師警告説,在關於雷尼替丁與癌症之間聯繫的爭論解決之前,美國的全科醫生可能會不願開處方給患者服用這種藥物。
分析師報告發布後,葛蘭素史克的公共關係負責人傑夫·波特警告不要過度反應。他給首席執行官保羅·吉羅拉米(當時還不是保羅爵士)、董事會主席奧斯汀·拜德(已經是奧斯汀爵士)和其他董事會成員寫了備忘錄。波特在備忘錄中承諾:“我們將密切關注形勢,以便在情況惡化時提出迅速的防禦行動。”後來,在一份證詞中,當時擔任葛蘭素史克臨牀研究副主任的高管會説,董事會從未要求他測試雷尼替丁是否會形成亞硝胺化合物。
葛蘭素史克對澤泰可潛在癌症風險的瞭解
在1981年夏天的英國一項試驗中,11名健康男性每天早晚各服用150毫克雷尼替丁,連續四周。葛蘭素科學家想要看看長期使用雷尼替丁是否會影響胃部細菌,特別是可能產生更多亞硝酸鹽的細菌,從而可能形成亞硝胺。他們發現確實會。他們得出的結論是這一點的重要性並不清楚。後來由FDA審查的一份總結中,葛蘭素科學家寫道,是的,高水平的亞硝酸鹽可以形成亞硝胺,幾乎所有亞硝胺都是致癌物質。但迄今為止進行的動物研究並未表明雷尼替丁是致癌的,因此無法估計人類的風險水平。此外,患者不應長期服用這種藥物。“雷尼替丁僅推薦短期使用,”科學家得出結論,“因此,如果有的話,致癌風險應該被最小化。”
許多人最終會服用澤地高達數月,有時甚至數年,甚至幾十年。
1981年10月,葛蘭素史克宣佈計劃在北卡羅來納州建立一家工廠,生產澤地高。這種藥物已經在英國和意大利銷售。研究人員正在研究它。熱那亞大學的Silvio De Flora在英國醫學雜誌《柳葉刀》上發表了他的研究結果,顯示當雷尼替丁與亞硝酸鹽混合時,結果是“有毒和誘變作用”。De Flora並沒有試圖找出毒性的原因;他後來建議任何被開處方澤地高的人限制他們對亞硝酸鹽的攝入,並在飯前或飯後服用這種藥物。全球範圍內,預防胃灼熱的澤地高服用説明會建議在餐後不久使用。
葛蘭素史克的高管立即與De Flora取得聯繫。“他們試圖説服我們雷尼替丁的安全性,”他在電子郵件中説。“製藥公司不喜歡這種研究。”
五名葛蘭素史克科學家兩週後在《柳葉刀》上發表了一封信,他們説,為了讓De Flora的發現有所依據。他們指出De Flora使用的亞硝酸鹽濃度在人類胃中永遠不會找到。這成為了葛蘭素史克的標準論點。De Flora説,研究人員通常在實驗室實驗中使用高劑量的試驗化合物,“因為他們評估給定效果的時間短,而不像更常見的情況是長時間暴露於低劑量。”
1982年3月,葛蘭素史克得知另一項研究揭示了雷尼替丁的潛在危險。這份僅有幾頁長的報告是由其競爭對手史密斯克萊恩和法國製藥公司(生產泰力美)發送給該公司的。那裏的研究人員還將雷尼替丁與不同濃度的亞硝酸鹽結合,並觀察到了毒素的形成。他們以葛蘭素史克的名義命名:NDMA。
在葛蘭素史克公司持懷疑態度是很自然的。一家公司測試了一種競爭產品並發現了一個缺陷。葛蘭素史克要求其中一位科學家進行自己的測試:理查德·坦納,他在生化藥理學部門工作。他得到了相同的結果。他在一些樣本中發現了高達232,000納克的NDMA。後來,當美國食品藥品監督管理局認為任何藥物中含有微量的NDMA是可以接受的時,這個數量是96納克。坦納在使用較低的亞硝酸鹽水平時沒有發現NDMA,而公司現在表示這更接近於實際人類胃部的條件。但是根據1982年的法庭文件顯示,葛蘭素史克公司保密了這項研究。美國臨牀研究副主任從未被告知坦納的報告。胃腸研究的高級醫學顧問也不知情。美國食品藥品監督管理局也不知情。
 葛蘭素史克公司將坦納報告保密了將近四十年。來源:GSK,Zantac(雷尼替丁)產品責任訴訟葛蘭素史克公司還知道雷尼替丁存在另一個潛在嚴重問題。它不總是穩定的。這種藥物對熱和濕度敏感,當暴露在過多的熱或濕度下時會分解。這正是美國食品藥品監督管理局後來關注的內容:在某些條件下,不一定是極端條件,有時是正常室温下,雷尼替丁開始分解。這為藥物本身形成NDMA創造了條件。
葛蘭素史克公司將坦納報告保密了將近四十年。來源:GSK,Zantac(雷尼替丁)產品責任訴訟葛蘭素史克公司還知道雷尼替丁存在另一個潛在嚴重問題。它不總是穩定的。這種藥物對熱和濕度敏感,當暴露在過多的熱或濕度下時會分解。這正是美國食品藥品監督管理局後來關注的內容:在某些條件下,不一定是極端條件,有時是正常室温下,雷尼替丁開始分解。這為藥物本身形成NDMA創造了條件。
1982年公司的一次交流集中在防止注射用雷尼替丁分解上。葛蘭素剛剛提交了銷售雷尼替丁片劑的申請,並很快將尋求注射劑的批准。製藥開發部主管約翰·帕德菲爾德堅持認為這種版本的雷尼替丁必須保持在4攝氏度(39華氏度)以下,從英國運往美國,運輸到美國各地並存放在區域倉庫。他在3月寫道,不這樣做將是“非常危險的事情。” 幾個月後,在7月的備忘錄中,公司高管寫道:“注射劑的冷藏對葛蘭素的營銷是不可接受的。” 帕德菲爾德堅持認為。“這種產品對温度非常敏感,”他回信道。“我們已經討論過,保護產品是至關重要的。”
在北卡羅來納州,事情發展迅速。美國對雷尼替丁的第一批人體試驗是在格拉克索公司於1982年3月提交新藥申請之前僅僅兩年前開始的。但是當時的臨牀研究副主任弗雷德·埃舍爾曼説,公司規模小,員工年輕,他們從不妥協安全,也不必處理大量的官僚主義。“每個人都認為這是一種很棒的藥物,”他説。“我們越快將其推向市場,患者就能越快使用。我們都致力於做好事情。”埃舍爾曼是許多人中應該看到坦納研究報告但沒有看到的人之一。他現在不想對此發表評論,但他説:“如果這種藥物本身有毒,我們早就會發現了。”
原告律師:在這個行業中,這種速度是完全聞所未聞的。
弗雷德·埃舍爾曼:是的,先生。
律師:那麼,可以説雷尼替丁的臨牀開發是以非常快速且需要大量工作的狂熱步伐進行的嗎?
埃舍爾曼:可以這麼説。
—證詞,2021年5月
 插圖:伊布拉欣·雷因塔卡斯為彭博商業週刊1982年5月,埃舍爾曼和一羣格拉克索的科學家在國家醫學圖書館的一個房間裏向一組獨立研究人員和一羣FDA官員介紹了贊特克的案例。該小組將推薦FDA是否應該批准該藥在美國銷售。
插圖:伊布拉欣·雷因塔卡斯為彭博商業週刊1982年5月,埃舍爾曼和一羣格拉克索的科學家在國家醫學圖書館的一個房間裏向一組獨立研究人員和一羣FDA官員介紹了贊特克的案例。該小組將推薦FDA是否應該批准該藥在美國銷售。
大衞·傑克,曾幫助發現雷尼替丁的人,首先發言。他指出公司對雷尼替丁進行了廣泛的毒理學研究,並未發現任何問題。但在那天早上,他説,“我們只想專注於引起一些人擔憂的部分,即這類藥物可能導致癌症的可能性。” 他和其他葛蘭素史克的科學家展示了三項研究,表明長期使用雷尼替丁(大約兩年)並不會導致大鼠或小鼠患癌症。“雷尼替丁被證明是一種非常無毒的化合物,”傑克的一位同事説。“沒有證據表明雷尼替丁在胃部或其他任何地方本身具有致癌性。”
葛蘭素史克的科學家駁斥了雷尼替丁在任何正常人類條件下會形成亞硝胺的觀點。他們沒有提及公司的坦納研究。理查德·克萊恩在FDA工作了40多年,包括與藥物批准團隊合作(儘管沒有參與贊他可的審批),他説,如果機構瞭解坦納研究,可能至少會“激發FDA提出更多問題,要求更多數據。這可能會引起FDA的懷疑。”
事實上,討論已經超越了對癌症的任何擔憂,轉向了具體的用藥劑量和贊他可將治療的潰瘍類型。關於藥物需要如何運輸和儲存,以及標籤上是否應該有任何警告,幾乎沒有討論。討論進行得很快。午餐休息前,外部專家投票建議FDA批准這種藥物:每天150毫克,每次兩次,最多治療八週,用於治療急性十二指腸潰瘍,這是最常見的類型。最終標籤將包括指示將藥丸存放在家中不超過86華氏度的乾燥地方。一年後,即1983年5月,FDA批准葛蘭素出售贊他可。《紐約時報寫道,這種藥物已在31個國家銷售,比泰格美更強大幾倍,據説副作用更少,儘管這兩種藥物被認為非常安全,醫生已經為更廣泛範圍的胃部問題開過這兩種藥物,而不僅僅是公司建議的範圍。
 Zantac的初次美國批准,是在1983年。來源:美國食品和藥物管理局Zantac在美國的第一年銷售額約為1.25億美元,使其成為有史以來最成功的藥物推出之一。“弗雷德·埃舍爾曼因Zantac而成為葛蘭素史克的英雄,”北卡羅來納州的藥理學家喬·格雷登説,他是消費者健康組織人民藥房的聯合創始人。“葛蘭素史克的負責人説,‘Zantac是拉動火車的引擎。’它是賺錢的機器,是巨頭殺手。” 埃舍爾曼後來創辦了自己的公司,為製藥公司進行新藥試驗。幾名葛蘭素史克的高管加入了他。他在2011年以39億美元出售了這家企業,並後來向北卡羅來納大學教堂山分校的藥學院捐贈了1億美元。該學院已經以他的名字命名。
Zantac的初次美國批准,是在1983年。來源:美國食品和藥物管理局Zantac在美國的第一年銷售額約為1.25億美元,使其成為有史以來最成功的藥物推出之一。“弗雷德·埃舍爾曼因Zantac而成為葛蘭素史克的英雄,”北卡羅來納州的藥理學家喬·格雷登説,他是消費者健康組織人民藥房的聯合創始人。“葛蘭素史克的負責人説,‘Zantac是拉動火車的引擎。’它是賺錢的機器,是巨頭殺手。” 埃舍爾曼後來創辦了自己的公司,為製藥公司進行新藥試驗。幾名葛蘭素史克的高管加入了他。他在2011年以39億美元出售了這家企業,並後來向北卡羅來納大學教堂山分校的藥學院捐贈了1億美元。該學院已經以他的名字命名。
它是安全的。它有效。結束。
—弗雷德·埃舍爾曼的葛蘭素史克辦公室裏紀念Zantac獲得FDA批准的牌匾
葛蘭素史克的營銷活動是一次精彩的努力,旨在削弱當時全球最暢銷處方藥Tagamet。高管們知道Zantac每片含有的活性成分比Tagamet多,因此他們將其營銷為更有效。他們知道患者會被開具Zantac兩次,而不是四次。他們向醫生強調Zantac更方便。他們知道一些患者在使用Tagamet時會出現副作用——不良藥物相互作用和精神混亂。他們將Zantac營銷為更安全。而葛蘭素史克將Zantac的價格定得更高,比Tagamet高出15%到25%,作為其優於Tagamet的證據。史密斯、克萊因和法國公司則以自己的Tagamet宣傳活動作為回應,稱自己是潰瘍專家。
葛蘭素史克通過與瑞士藥企羅氏合作,將其銷售團隊擴大了三倍。當時,羅氏公司擁有龐大的員工隊伍,但沒有大型藥品。他們開始向胃腸科醫生推廣贊特,這是可以預料的,然後意外地開始為全科醫生、骨科醫生和藥劑師舉辦“教育研討會”。
贊特在美國推出三年後,美國食品藥品監督管理局(FDA)指責葛蘭素史克多次發佈虛假宣傳聲明,最近一次是在尋求符合政府報銷計劃資格時。“我們顯然在促使貴公司自願糾正這些廣告和促銷做法方面取得了很少的成功,”FDA在1986年5月的一封四頁信函中寫道。信函以監管行動的威脅結束。葛蘭素史克回應稱,該機構誤解了其行動。
那一年,泰力美成為首個銷售額達十億美元的藥品。次年,贊特超過了泰力美。
1988年3月,葛蘭素委託蓋洛普進行了一項名為“美國各地的胃灼熱”的民意調查。調查發現44%的成年人每月都會患胃灼熱。當時贊特可以用於治療胃灼熱,但也有很多無需處方的抗酸藥可供選擇。葛蘭素在電視和印刷媒體上推廣了這項調查。廣告指出,胃灼熱和慢性反流的其他症狀可能預示着潰瘍等疾病,並建議就醫。
北卡羅來納州一位備受尊敬的胃腸科醫生在1988年冬季進行了一項研究,顯示贊特可以幫助減輕跑步者的胃灼熱:一個新的潛在患者羣體,患有新命名的問題,即跑步者反流。這項研究規模較小,從未經過同行評議,但該醫生的聲望以及葛蘭素的公關機構確保了它受到關注。《紐約時報》後來報道稱,該醫生是葛蘭素的有薪顧問。他表示,他認為葛蘭素不會利用這項研究。
到了1989年,Zantac的價值達到了20億美元。它佔了Glaxo銷售額的一半,以及處方潰瘍藥市場的53%。
1993年,FDA對Zantac的營銷發出了威脅。該機構在一封警告信中表示,Glaxo進行了一系列傳播有誤導性信息的行為,聲稱Zantac在廣告和促銷中優於Tagamet。該機構要求Glaxo給美國醫生寫信,並在12家主要醫學期刊上發佈廣告,以糾正任何此類聲明。一位FDA發言人告訴倫敦的*《星期日泰晤士報》*,“大多數公司在推廣材料中不會犯錯誤,這是最糟糕的情況。” 兩個月後,Glaxo發佈了“糾正廣告”活動。
Glaxo有許多理由與FDA合作。其中之一是他們正在研發低劑量的Zantac非處方藥,用於治療心灼熱。FDA需要批准。高管們考慮為新藥片做的其他改變之一是它們的顏色。在一些穩定性測試中,這些藥片,原本是白色的,變成了黃色和棕色。Glaxo想要掩蓋這一點。他們決定為新藥片塗上一層粉紅色的塗層,由氧化鐵製成。變色通常是藥片正在惡化的跡象。在某些情況下,惡化可能導致危險的雜質形成。Glaxo表示Zantac沒有這種情況發生。正在研發非處方藥版本的伊恩·温特伯恩在一份證詞中説:“顏色被用於藥片的塗層,以確保藥片在整個貨架壽命內外觀一致。關於顏色變化與惡化相關的擔憂是不存在的。”
當葛蘭素史克完成申請 Zantac 的非處方藥申請時,Winterborn 是眾多收件人之一,收到了一封祝賀的電子郵件。“這標誌着我認為在過去兩年半中參與這個項目的每個人都做出了英勇的努力,”一位高管在1994年底寫道。“我認為這是葛蘭素史克有史以來最重要的成就之一。”
1996年春天,葛蘭素史克慶祝推出了 Zantac 75mg 的非處方藥片。它是粉色的,可以每天一次或兩次服用。美國人每年已經花費大約十億美元用於緩解胃灼熱。葛蘭素史克的營銷人員已經準備好了。他們的口號是:“傳奇延續。”
Zantac 的成分中沒有任何東西使它成為一個價值十億美元的藥物。我們讓它成為了那種產品。
—保羅·吉羅拉米,葛蘭素史克董事會主席,在*《金融時報》*,1988年
1995年,葛蘭素史克完成了對另一家英國藥企威康公司的敵意收購。五年後,2000年,葛蘭素史克威康收購了其長期競爭對手,當時被稱為史密斯克萊因·比奇姆的公司。這是該行業歷史上最大的合併,也創造了世界上最大的藥企,葛蘭素史克。
 詹姆斯·戈茨的案件將成為州法院審理的第一個案件。攝影師:傑西卡·龐斯,攝於彭博商業週刊那時,詹姆斯·戈茨,一名居住在南加利福尼亞的航空工程師,已經服用 Zantac 多年:先是處方藥,然後是非處方藥。在FDA批准了仿製藥版本後,他也服用了那些藥物。約翰·拉塞爾,居住在洛杉磯附近,被診斷患有胃炎,並從當地加油站和藥店購買了這種藥物。
詹姆斯·戈茨的案件將成為州法院審理的第一個案件。攝影師:傑西卡·龐斯,攝於彭博商業週刊那時,詹姆斯·戈茨,一名居住在南加利福尼亞的航空工程師,已經服用 Zantac 多年:先是處方藥,然後是非處方藥。在FDA批准了仿製藥版本後,他也服用了那些藥物。約翰·拉塞爾,居住在洛杉磯附近,被診斷患有胃炎,並從當地加油站和藥店購買了這種藥物。
Zantac的變色問題仍然存在。2010年,GSK的基因毒性風險評估負責人安德魯·西爾被要求調查為什麼Zantac的注射劑變黃。西爾的調查測試了已知會導致這種黃色變色的雜質。實驗室中使用的NDMA是黃色的,但他沒有對其進行測試。這個問題在2015年再次出現,當時中國的一個生產基地報告稱Zantac片劑出現了變色和降解問題。GSK給醫生們發了一封信,聲明公司尚未能確定任何特定的雜質,但無法確認這些棕色變色的片劑是否符合其安全標準。沒有人尋找NDMA。在一次證詞中,西爾將問題歸咎於不當存儲。
在這兩起事件之間,還發生了另外兩起與Zantac無關的事件,給GSK帶來了不必要的審查。2012年,該公司同意認罪並支付30億美元罰款,原因是將藥物用於不當用途,無視安全數據並欺騙醫療補助計劃。這些藥物是繼Zantac之後該公司最受歡迎的藥物:帕羅西汀、威而鋁和糖尿病藥物阿凡迪亞。美國司法部稱其為美國歷史上最大的醫療欺詐和制裁,並是藥品公司有史以來支付的最大金額。兩年後,中國對GSK處以5億美元罰款,並驅逐了一名賄賂醫生開處方的高管。該公司告訴BBC,他們已向中國政府和人民“發表了一份道歉聲明”。
原告律師:已知在高温條件下,雷尼替丁會分解嗎?
安迪·懷特黑德,第二代研發總監:這在80年代的開發過程中應該是已知的。
律師:那麼什麼時候已知雷尼替丁在受潮時會分解?
懷特黑德:這應該是最初的開發工作的一部分。
律師:所以雷尼替丁在高温和潮濕條件下會分解這一點幾乎已經有40年的歷史了?
懷特黑德:是的,因為這是作為開發的一部分而調查的水解途徑。
—證詞,2022年5月
Goetz在2017年被診斷患有膀胱癌時已經60歲了。這本身並不太不尋常;60歲是男性經常被診斷出患有這種特定癌症的年齡。吸煙者會患上膀胱癌,但Goetz自22歲以來就沒有吸煙過。他的工作也沒有讓他接觸到任何潛在有害化學物質。這讓人困惑,但他沒有理由認為自己患癌症是其他原因造成的。不幸,可怕,但是隨機的。他的醫生刮除了腫瘤,並用免疫療法治療了他。然後他們等待。癌症很可能會復發,而且一旦復發就會很具侵略性。醫生不得不切除Goetz的膀胱和前列腺以及20英尺的腸道。手術後,他患上了腎結石和敗血症。Goetz將是成千上萬人中第一個參加對GSK的審判。因此,他的律師拒絕讓他就本文發表評論。
GSK最終交出了自1982年以來一直被擱置的報告
2019年9月,FDA收到了一份19頁的文件,其中提出了一些令人擔憂的聲明關於雷尼替丁。Valisure,一家獨立於FDA運營的私人實驗室表示,在Zantac和幾種雷尼替丁的仿製藥中發現了極高水平的NDMA。Valisure在一年前開始測試NDMA,當時FDA首次召回了被污染的血壓藥物纈沙坦的批次。這種情況似乎更糟。Valisure在測試的每個版本的雷尼替丁中發現了NDMA,並得出結論認為問題是分子本身固有的。
美國食品藥品監督管理局發佈了警報,但也質疑了Valisure使用的測試方法。該機構表示將按照自己的方案進行測試。一個月內,至少有二十多個國家從商店撤回了雷尼替丁或停止了其分發。當時已經將在美國銷售Zantac的權利出售給了GSK,該公司自行停止了該藥物的供應。法國公司Sanofi,於2017年從Boehringer Ingelheim GmbH手中獲得了美國的權利,以及從1998年到2006年銷售Zantac的輝瑞公司也採取了同樣的行動。
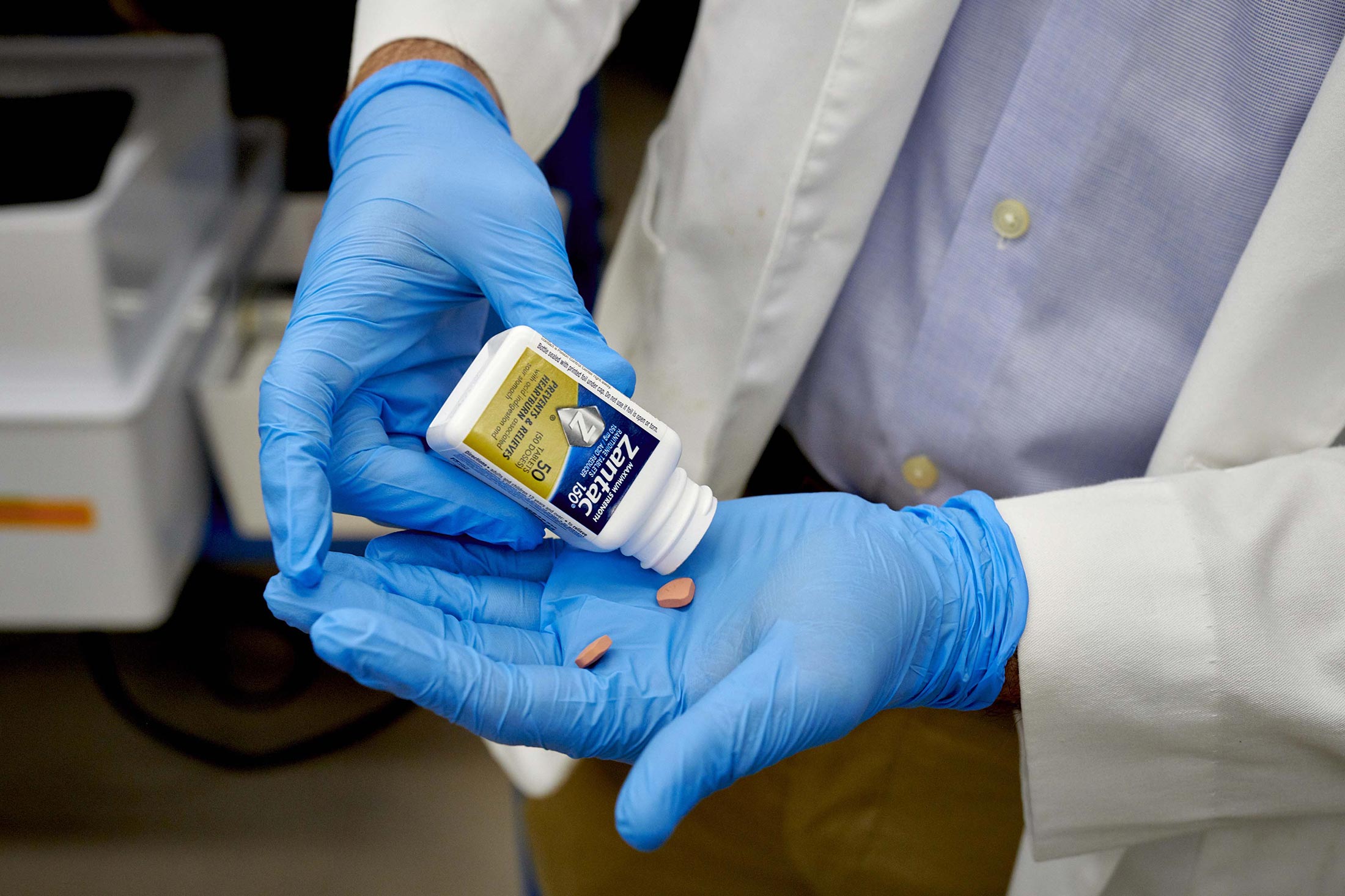 科學家在Valisure測試了Zantac,該公司在2019年向FDA提出了擔憂。攝影師:Gabby Jones/Bloomberg
科學家在Valisure測試了Zantac,該公司在2019年向FDA提出了擔憂。攝影師:Gabby Jones/Bloomberg 攝影師:Gabby Jones/Bloomberg“大家,我們迫切需要確定以下研究報告是否已提交給歐盟和美國,”GSK的一位高級執行官在去年11月寫信給同事們。她談論的是Tanner報告,答案是否定的,它並沒有作為任何新藥申請的一部分提交。最終,GSK交出了這份自1982年以來一直被擱置的報告。
攝影師:Gabby Jones/Bloomberg“大家,我們迫切需要確定以下研究報告是否已提交給歐盟和美國,”GSK的一位高級執行官在去年11月寫信給同事們。她談論的是Tanner報告,答案是否定的,它並沒有作為任何新藥申請的一部分提交。最終,GSK交出了這份自1982年以來一直被擱置的報告。
美國食品藥品監督管理局在2020年4月做出了罕見而激烈的決定:強迫雷尼替丁的製造商——任何版本、任何劑量——停止生產和銷售這種藥物。雷尼替丁完蛋了。“即使在正常存儲條件下,雷尼替丁中的NDMA水平也會增加,”該機構表示。“在更高温度下存儲的樣本中,包括產品在分銷和消費者處理過程中可能暴露的温度下,NDMA的增加明顯。” People’s Pharmacy的Graedon稱這是“我們所知道的第一個存儲條件對藥物質量產生深遠影響的例子,而FDA已經承認了這一點。”
直到2021年10月,美國食品藥品監督管理局才分享了一些關於該機構檢測到的具體信息,而且這並不是在一篇發表的論文中,而是在一個名為FDA Grand Rounds的月度講座系列中。該機構表示,一片冷薄荷味的雷尼替丁最初被檢測出含有357納克的NDMA,幾乎是FDA規定的任何藥物中限量的四倍,五個月後達到了931納克。
美國食品藥品監督管理局拒絕就其與葛蘭素史克公司的任何互動發表評論,但在一份聲明中表示,該機構致力於提供安全、有效和質量上乘的藥物,根據當時的科學評估利弊,“當新的雜質被識別出來、新的製造工藝被採用或者當科學取得進展時,FDA致力於改善安全性、質量和有效性,並將繼續調查對患者健康構成潛在風險的問題。” FDA決定將雷尼替丁從市場上撤出是基於NDMA在藥物中的形成,而不是在胃中。該機構表示,一旦被攝入,雷尼替丁不會導致更多的NDMA形成。一些科學家持不同意見。
2020年12月,葛蘭素史克公司發佈了所謂的根本原因分析結果。這是一個無定論的結果:公司的科學家無法確定NDMA是如何在雷尼替丁中形成的,並指出在20世紀70年代,當這種藥物首次開發時,沒有人能夠合理地預測NDMA會形成。
六個月後,美國食品藥品監督管理局做出了另一個罕見且具有重大影響的決定。儘管在雷尼替丁中發現了NDMA,儘管雷尼替丁是一種可能的人類致癌物,但該機構表示沒有“一致的信號”表明澤靈增加了患癌風險。這是在一份10頁的研究中第8頁上的説法,該研究檢查了服用雷尼替丁的人尿液中的NDMA水平。該聲明依賴於外部科學家的七篇論文。其中一篇顯示了雷尼替丁與乳腺癌之間的聯繫,但該機構批評了其方法。第二篇提出了有關肝癌的擔憂,儘管作者表示他們尚沒有足夠的數據來證實這種聯繫。看起來FDA的結論並不是明確的,但這份聲明現在已成為葛蘭素史克公司公關和可能也是法律辯護的一個常規部分。“無罪推定”是一些科學家稱之的。自那時以來,已有三項研究發現了這種藥物與癌症之間的聯繫,尤其是膀胱癌和肝癌。FDA表示堅持其聲明,批評者稱這也為允許一種危險化學物質潛伏在藥物中幾十年而免責。
“我只希望我對我們開發Zantac時進行的所有問題和研究有更好的記憶。當時有關亞硝胺的擔憂,我知道當時進行了終身致癌性研究。”
—Ian Winterborn,在一次證詞中朗讀的電子郵件,2022年5月
過了一段時間,約翰·拉塞爾服用的非處方Zantac藥丸已經無法緩解他的不適,2017年一位醫生開了每天300毫克的劑量。一年半後,拉塞爾發現尿液中有血。一位醫生在他的膀胱中發現了一個3釐米的腫瘤。像戈茨一樣,拉塞爾被告知癌症很可能會復發,而事實也確實如此。他説:“這就像一株雜草。”拉塞爾的家庭醫生感到困惑,拉塞爾説:“我從來沒有抽煙——那是最高的風險因素——我從來沒有接觸化學品或塑料。我與癌症沒有遺傳關係。我幾乎沒聽説過膀胱癌。”自2021年以來,拉塞爾進行的每次膀胱鏡檢查都顯示出腫瘤;在過去的18個月裏,他接受了四次手術。
當他得知Zantac被召回時,他想:“我吃了成千上萬顆那種藥丸。”拉塞爾曾參加大學橄欖球比賽;鍛鍊曾經是他的愛好。但現在,58歲的他因手術和擔憂而虛弱。“我想要找到罪魁禍首,”他説。拉塞爾在去年12月讀到了聯邦法官的裁決。“我想要在法庭上説話,”他説。“我想讓法官告訴我他們認為我的癌症是從哪裏來的。”
詹姆斯·戈茨的腎功能正在衰竭,很快他將需要透析,但他能夠工作,並期望在阿拉米達縣的法庭上作證。當Zantac被召回時,他保留了已經購買的四瓶藥。它們存放在他的一位律師布倫特·維斯納的辦公室的冰箱裏,拉塞爾剩下的藥片也在那裏。維斯納説,檢測顯示戈茨的一顆藥丸中含有3000納克的NDMA,拉塞爾的一顆含有兩倍多。維斯納説他邀請了GSK來測試這些藥片,但公司並未這樣做。
拜林格(Boehringer)、輝瑞(Pfizer)和賽諾菲(Sanofi)在12月份解決了Goetz的案件;解決金額保密。GSK也可能會解決。如果不解決,Wisner和他在該案中的合作伙伴Jennifer Moore將在同一法院進行審理,Wisner曾代表一對聲稱除草劑Roundup導致他們患癌症的夫婦贏得了20億美元的判決。後來法官將判決降至8700萬美元。
Moore還為Roundup訴訟中的客户贏得了鉅額判決。她表示,在除草劑案中,關於它是否致癌並沒有科學共識,而NDMA被承認是危險的。“在這裏,每個科學組織、每個監管機構都表示NDMA對人類是致癌的,”她説。“而在這裏,我們自己客户的藥片顯示存在癌原物質含量極高。”
Goetz審判具有特殊意義,因為它是在佛羅里達州聯邦裁決後的第一個審判。當時公司和投資者都感到危險已經過去。“顯然,我們對結果感到高興,”GSK的首席執行官Emma Walmsley在2月1日的盈利電話會議上説。
根據GSK的説法,羅森伯格對13項流行病學研究進行了審查,未發現雷尼替丁與任何癌症之間的聯繫。但事實並非如此:她審查了11項研究,其中有四項發現了科學家認為值得進一步研究的關聯。羅森伯格評估的許多研究都涉及總體癌症風險。Wisner表示,結合包含膀胱癌數據的流行病學研究的分析,包括羅森伯格考慮過的一些研究,顯示“如果服用雷尼替丁,存在明顯升高的風險。”
科學界普遍認為,這個問題尚未解決。不同的法官和陪審團可能會得出不同的結論。GSK可能會在加利福尼亞、特拉華州和其他州面臨數年的訴訟,可能會面臨數十億美元的賠償。估計的金額從35億美元到170億美元不等。該公司還在2020年7月披露,正在配合司法部對贊他康相關調查。
輝瑞和賽諾菲面臨類似的法律訴訟,指控它們銷售一種潛在危險的產品。與GSK一樣,它們否認贊他康構成任何健康威脅。在被要求發表評論時,輝瑞提到了其網站上的一份聲明,指出公司在2006年最後一次銷售贊他康,並表示“我們對這項訴訟有重大的辯護措施,法院還有重大的法律和事實問題需要解決。”賽諾菲發言人表示:“鑑於原告主張缺乏科學支持,賽諾菲對我們在整個訴訟過程中的辯護仍然充滿信心。”
賽諾菲進行了自己的調查,研究了贊他康片劑中NDMA是如何形成的,希望這樣做可以做出一些改變,以經得起FDA的審查,並將這種藥物重新推向市場。該公司稱這一努力為“丘吉爾計劃”。這導致了一個意想不到的結果,這個結果促使做出了一個前所未有的決定。賽諾菲無法找到一種可接受的方法來製造含有定義贊他康、雷尼替丁這種成分的贊他康。
相反,2021年,該公司重新配製了含有法莫替丁的贊塔克,這種活性成分已經定義了另一種胃灼熱藥物,貝普胃藥。新的贊塔克現在已經上市。在其網站上,賽諾菲描述這個藥物版本為“在贊塔克品牌的建立歷史和傳統基礎上發展”。
“等一下,你是在告訴我他們正在推廣OTC法莫替丁並稱其為贊塔克?我顯然感到困惑。我不知道該怎麼看待這件事。”
—弗雷德·埃舍爾曼在一份證詞中,2021年5月
閲讀下一篇: 雀巢的6000美元花生過敏藥丸一無是處